МЕТАБОЛИЗМ | Энциклопедия Кругосвет
Содержание статьиМЕТАБОЛИЗМ, или обмен веществ, химические превращения, протекающие от момента поступления питательных веществ в живой организм до момента, когда конечные продукты этих превращений выделяются во внешнюю среду. К метаболизму относятся все реакции, в результате которых строятся структурные элементы клеток и тканей, и процессы, в которых из содержащихся в клетках веществ извлекается энергия. Иногда для удобства рассматривают по отдельности две стороны метаболизма – анаболизм и катаболизм, т.е. процессы созидания органических веществ и процессы их разрушения. Анаболические процессы обычно связаны с затратой энергии и приводят к образованию сложных молекул из более простых, катаболические же сопровождаются высвобождением энергии и заканчиваются образованием таких конечных продуктов (отходов) метаболизма, как мочевина, диоксид углерода, аммиак и вода.
Термин «обмен веществ» вошел в повседневную жизнь с тех пор, как врачи стали связывать избыточный или недостаточный вес, чрезмерную нервозность или, наоборот, вялость больного с повышенным или пониженным обменом.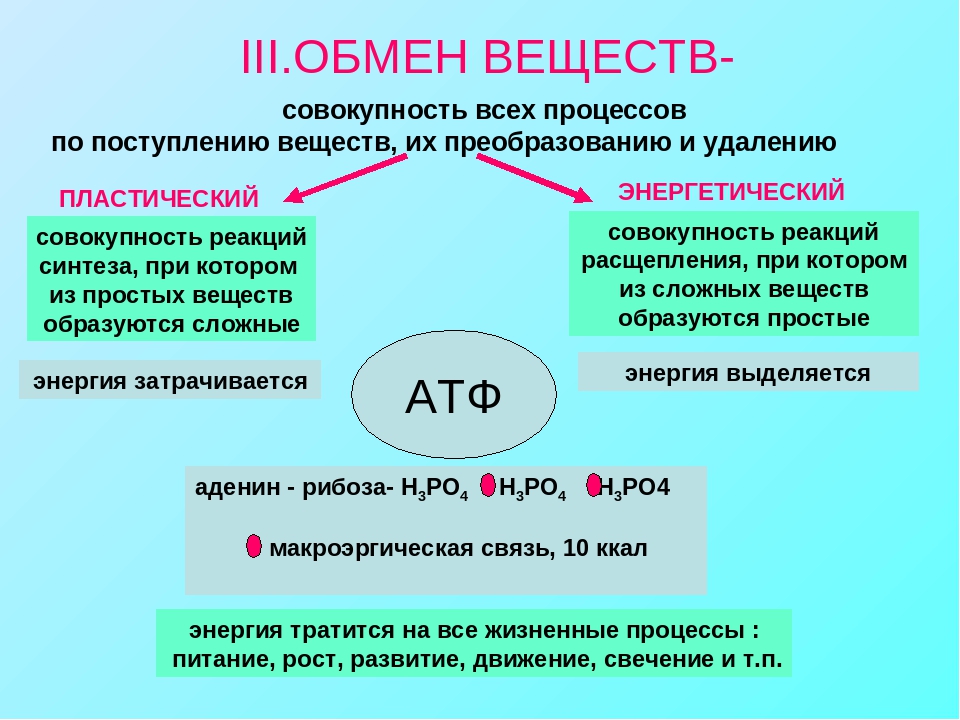
Методы исследования.
При изучении метаболизма какого-нибудь одного из питательных веществ прослеживают все его превращения от той формы, в какой оно поступает в организм, до конечных продуктов, выводимых из организма. В таких исследованиях применяется крайне разнообразный набор биохимических методов.
Использование интактных животных или органов.

Животному вводят изучаемое соединение, а затем в его моче и экскрементах определяют возможные продукты превращений (метаболиты) этого вещества. Более определенную информацию можно получить, исследуя метаболизм определенного органа, например печени или мозга. В этих случаях вещество вводят в соответствующий кровеносный сосуд, а метаболиты определяют в крови, оттекающей от данного органа.
Поскольку такого рода процедуры сопряжены с большими трудностями, часто для исследования используют тонкие срезы органов. Их инкубируют при комнатной температуре или при температуре тела в растворах с добавкой того вещества, метаболизм которого изучают. Клетки в таких препаратах не повреждены, и так как срезы очень тонкие, вещество легко проникает в клетки и легко выходит из них. Иногда затруднения возникают из-за слишком медленного прохождения вещества сквозь клеточные мембраны. В этих случаях ткани измельчают, чтобы разрушить мембраны, и с изучаемым веществом инкубируют клеточную кашицу.
Использование клеток.
Даже клетки представляют собой очень сложно организованные системы. В них имеется ядро, а в окружающей его цитоплазме находятся более мелкие тельца, т.н. органеллы, различных размеров и консистенции. С помощью соответствующей методики ткань можно «гомогенизировать», а затем подвергнуть дифференциальному центрифугированию (разделению) и получить препараты, содержащие только митохондрии, только микросомы или прозрачную жидкость – цитоплазму. Эти препараты можно по отдельности инкубировать с тем соединением, метаболизм которого изучается, и таким путем установить, какие именно субклеточные структуры участвуют в его последовательных превращениях. Известны случаи, когда начальная реакция протекает в цитоплазме, ее продукт подвергается превращению в микросомах, а продукт этого превращения вступает в новую реакцию уже в митохондриях.
Использование радиоактивных изотопов.
Для изучения метаболизма какого-либо вещества необходимы: 1) соответствующие аналитические методы для определения этого вещества и его метаболитов; и 2) методы, позволяющие отличать добавленное вещество от того же вещества, уже присутствующего в данном биологическом препарате. Эти требования служили главным препятствием при изучении метаболизма до тех пор, пока не были открыты радиоактивные изотопы элементов и в первую очередь радиоактивный углерод  Эта же методика позволяет легко отличать молекулы радиоактивной жирной кислоты, введенной экспериментатором, от молекул жирной кислоты, уже присутствовавших в митохондриях к началу эксперимента.
Эта же методика позволяет легко отличать молекулы радиоактивной жирной кислоты, введенной экспериментатором, от молекул жирной кислоты, уже присутствовавших в митохондриях к началу эксперимента.
Хроматография и электрофорез.
В дополнение к вышеупомянутым требованиям биохимику необходимы и методы, позволяющие разделять смеси, состоящие из малых количеств органических веществ. Важнейший из них – хроматография, в основе которой лежит феномен адсорбции. Разделение компонентов смеси проводят при этом либо на бумаге, либо путем адсорбции на сорбенте, которым заполняют колонки (длинные стеклянные трубки), с последующей постепенной элюцией (вымыванием) каждого из компонентов.
Разделение методом электрофореза зависит от знака и числа зарядов ионизированных молекул. Электрофорез проводят на бумаге или на каком-нибудь инертном (неактивном) носителе, таком, как крахмал, целлюлоза или каучук.
Высокочувствительный и эффективный метод разделения – газовая хроматография. Им пользуются в тех случаях, когда подлежащие разделению вещества находятся в газообразном состоянии или могут быть в него переведены.
Выделение ферментов.
Последнее место в описываемом ряду – животное, орган, тканевой срез, гомогенат и фракция клеточных органелл – занимает фермент, способный катализировать определенную химическую реакцию. Выделение ферментов в очищенном виде – важный раздел в изучении метаболизма.
Сочетание перечисленных методов позволило проследить главные метаболические пути у большей части организмов (в том числе у человека), установить, где именно эти различные процессы протекают, и выяснить последовательные этапы главных метаболических путей. К настоящему времени известны тысячи отдельных биохимических реакций, изучены участвующие в них ферменты.
Клеточный метаболизм.
Живая клетка – это высокоорганизованная система. В ней имеются различные структуры, а также ферменты, способные их разрушить. Содержатся в ней и крупные макромолекулы, которые могут распадаться на более мелкие компоненты в результате гидролиза (расщепления под действием воды). В клетке обычно много калия и очень мало натрия, хотя клетка существует в среде, где натрия много, а калия относительно мало, и клеточная мембрана легко проницаема для обоих ионов.
Потребность в энергии.
Чтобы удержать систему в состоянии, далеком от химического равновесия, требуется производить работу, а для этого необходима энергия. Получение этой энергии и выполнение этой работы – непременное условие для того, чтобы клетка оставалась в своем стационарном (нормальном) состоянии, далеком от равновесия. Одновременно в ней выполняется и иная работа, связанная со взаимодействием со средой, например: в мышечных клетках – сокращение; в нервных клетках – проведение нервного импульса; в клетках почек – образование мочи, значительно отличающейся по своему составу от плазмы крови; в специализированных клетках желудочно-кишечного тракта – синтез и выделение пищеварительных ферментов; в клетках эндокринных желез – секреция гормонов; в клетках светляков – свечение; в клетках некоторых рыб – генерирование электрических разрядов и т.
Источники энергии.
В любом из перечисленных выше примеров непосредственным источником энергии, которую клетка использует для производства работы, служит энергия, заключенная в структуре аденозинтрифосфата (АТФ). В силу особенностей своей структуры это соединение богато энергией, и разрыв связей между его фосфатными группами может происходить таким образом, что высвобождающаяся энергия используется для производства работы. Однако энергия не может стать доступной для клетки при простом гидролитическом разрыве фосфатных связей АТФ: в этом случае она расходуется впустую, выделяясь в виде тепла. Процесс должен состоять из двух последовательных этапов, в каждом из которых участвует промежуточный продукт, обозначенный здесь X–Ф (в приведенных уравнениях X и Y означают два разных органических вещества; Ф – фосфат; АДФ – аденозиндифосфат):
Поскольку практически для любого проявления жизнедеятельности клеток необходим АТФ, неудивительно, что метаболическая активность живых клеток направлена в первую очередь на синтез АТФ. Этой цели служат различные сложные последовательности реакций, в которых используется потенциальная химическая энергия, заключенная в молекулах углеводов и жиров (липидов).
Этой цели служат различные сложные последовательности реакций, в которых используется потенциальная химическая энергия, заключенная в молекулах углеводов и жиров (липидов).
МЕТАБОЛИЗМ УГЛЕВОДОВ И ЛИПИДОВ
Синтез АТФ.
Анаэробный (без участия кислорода).
Главная роль углеводов и липидов в клеточном метаболизме состоит в том, что их расщепление на более простые соединения обеспечивает синтез АТФ. Несомненно, что те же процессы протекали и в первых, самых примитивных клетках. Однако в атмосфере, лишенной кислорода, полное окисление углеводов и жиров до CO
В ходе 11 последовательных реакций, необходимых для того, чтобы завершилось это превращение, образуется ряд промежуточных продуктов, представляющих собой эфиры фосфорной кислоты (фосфаты). Их фосфатная группа переносится на аденозиндифосфат (АДФ) с образованием АТФ. Чистый выход АТФ составляет 2 молекулы АТФ на каждую молекулу глюкозы, расщепленную в процессе брожения. Аналогичные процессы происходят во всех живых клетках; поскольку они поставляют необходимую для жизнедеятельности энергию, их иногда (не вполне корректно) называют анаэробным дыханием клеток.
Их фосфатная группа переносится на аденозиндифосфат (АДФ) с образованием АТФ. Чистый выход АТФ составляет 2 молекулы АТФ на каждую молекулу глюкозы, расщепленную в процессе брожения. Аналогичные процессы происходят во всех живых клетках; поскольку они поставляют необходимую для жизнедеятельности энергию, их иногда (не вполне корректно) называют анаэробным дыханием клеток.
У млекопитающих, в том числе у человека, такой процесс называется гликолизом и его конечным продуктом является молочная кислота, а не спирт и CO2. Вся последовательность реакций гликолиза, за исключением двух последних этапов, полностью идентична процессу, протекающему в дрожжевых клетках.
Аэробный (с использованием кислорода).
С появлением в атмосфере кислорода, источником которого послужил, очевидно, фотосинтез растений, в ходе эволюции развился механизм, обеспечивающий полное окисление глюкозы до CO2 и воды, – аэробный процесс, в котором чистый выход АТФ составляет 38 молекул АТФ на каждую окисленную молекулу глюкозы. Этот процесс потребления клетками кислорода для образования богатых энергией соединений известен как клеточное дыхание (аэробное). В отличие от анаэробного процесса, осуществляемого ферментами цитоплазмы, окислительные процессы протекают в митохондриях. В митохондриях пировиноградная кислота – промежуточный продукт, образовавшийся в анаэробной фазе – окисляется до СО2 в шести последовательных реакциях, в каждой из которых пара электронов переносится на общий акцептор – кофермент никотинамидадениндинуклеотид (НАД). Эту последовательность реакций называют циклом трикарбоновых кислот, циклом лимонной кислоты или циклом Кребса. Из каждой молекулы глюкозы образуется 2 молекулы пировиноградной кислоты; 12 пар электронов отщепляется от молекулы глюкозы в ходе ее окисления, описываемого уравнением:
Этот процесс потребления клетками кислорода для образования богатых энергией соединений известен как клеточное дыхание (аэробное). В отличие от анаэробного процесса, осуществляемого ферментами цитоплазмы, окислительные процессы протекают в митохондриях. В митохондриях пировиноградная кислота – промежуточный продукт, образовавшийся в анаэробной фазе – окисляется до СО2 в шести последовательных реакциях, в каждой из которых пара электронов переносится на общий акцептор – кофермент никотинамидадениндинуклеотид (НАД). Эту последовательность реакций называют циклом трикарбоновых кислот, циклом лимонной кислоты или циклом Кребса. Из каждой молекулы глюкозы образуется 2 молекулы пировиноградной кислоты; 12 пар электронов отщепляется от молекулы глюкозы в ходе ее окисления, описываемого уравнением:
Перенос электронов.
В каждой митохондрии имеется механизм, посредством которого восстановленный НАД (НАДЧН, где Н – водород), образовавшийся в цикле трикарбоновых кислот, передает свою пару электронов кислороду. Перенос, однако, не происходит напрямую. Электроны как бы передаются «из рук в руки» и, лишь пройдя цепь переносчиков, присоединяются к кислороду. Эта «цепь переноса электронов» состоит из следующих компонентов:
Перенос, однако, не происходит напрямую. Электроны как бы передаются «из рук в руки» и, лишь пройдя цепь переносчиков, присоединяются к кислороду. Эта «цепь переноса электронов» состоит из следующих компонентов:
НАДНЧН ® Флавинадениндинклеотид ® Кофермент Q ®
® Цитохром b ® Цитохром c ® Цитохром a ® O2
Все компоненты этой системы, находящиеся в митохондриях, фиксированы в пространстве и сцеплены друг с другом. Такое их состояние облегчает перенос электронов.
В состав НАД входит никотиновая кислота (витамин ниацин), а в состав флавинадениндинуклеотида – рибофлавин (витамин B2). Кофермент Q представляет собой высокомолекулярный хинон, синтезируемый в печени, а цитохромы – это три разных белка, каждый из которых, подобно гемоглобину, содержит гемогруппу.
В цепи переноса электронов на каждую пару электронов, перенесенную от НАДЧН на O2, синтезируется 3 молекулы АТФ. Поскольку от каждой молекулы глюкозы отщепляются и передаются молекулам НАД 12 пар электронов, в общей сложности на каждую молекулу глюкозы образуется 3ґ12 = 36 молекул АТФ. Этот процесс образования АТФ в ходе окисления называется окислительным фосфорилированием.
Этот процесс образования АТФ в ходе окисления называется окислительным фосфорилированием.
Липиды как источник энергии.
Жирные кислоты могут использоваться в качестве источника энергии приблизительно так же, как и углеводы. Окисление жирных кислот протекает путем последовательного отщепления от молекулы жирной кислоты двууглеродного фрагмента с образованием ацетилкофермента A (ацетил-КоА) и одновременной передачей двух пар электронов в цепь переноса электронов. Образовавшийся ацетил-КоА – нормальный компонент цикла трикарбоновых кислот, и в дальнейшем его судьба не отличается от судьбы ацетил-КоА, поставляемого углеводным обменом. Таким образом, механизмы синтеза АТФ при окислении как жирных кислот, так и метаболитов глюкозы практически одинаковы.
Если организм животного получает энергию почти целиком за счет одного только окисления жирных кислот, а это бывает, например, при голодании или при сахарном диабете, то скорость образования ацетил-КоА превышает скорость его окисления в цикле трикарбоновых кислот. В этом случае лишние молекулы ацетил-КоА реагируют друг с другом, в результате чего образуются в конечном счете ацетоуксусная и b-гидроксимасляная кислоты. Их накопление является причиной патологического состояния, т.н. кетоза (одного из видов ацидоза), который при тяжелом диабете может вызвать кому и смерть.
В этом случае лишние молекулы ацетил-КоА реагируют друг с другом, в результате чего образуются в конечном счете ацетоуксусная и b-гидроксимасляная кислоты. Их накопление является причиной патологического состояния, т.н. кетоза (одного из видов ацидоза), который при тяжелом диабете может вызвать кому и смерть.
Запасание энергии.
Животные питаются нерегулярно, и их организму нужно как-то запасать заключенную в пище энергию, источником которой являются поглощенные животным углеводы и жиры. Жирные кислоты могут запасаться в виде нейтральных жиров либо в печени, либо в жировой ткани. Углеводы, поступая в большом количестве, в желудочно-кишечном тракте гидролизуются до глюкозы или иных сахаров, которые затем в печени превращаются в ту же глюкозу. Здесь из глюкозы синтезируется гигантский полимер гликоген путем присоединения друг к другу остатков глюкозы с отщеплением молекул воды (число остатков глюкозы в молекулах гликогена доходит до 30 000). Когда возникает потребность в энергии, гликоген вновь распадается до глюкозы в реакции, продуктом которой является глюкозофосфат. Этот глюкозофосфат направляется на путь гликолиза – процесса, составляющего часть пути окисления глюкозы. В печени глюкозофосфат может также подвергнуться гидролизу, и образующаяся глюкоза поступает в кровоток и доставляется кровью к клеткам в разных частях тела.
Этот глюкозофосфат направляется на путь гликолиза – процесса, составляющего часть пути окисления глюкозы. В печени глюкозофосфат может также подвергнуться гидролизу, и образующаяся глюкоза поступает в кровоток и доставляется кровью к клеткам в разных частях тела.
Синтез липидов из углеводов.
Если количество углеводов, поглощенных с пищей за один прием, больше того, какое может быть запасено в виде гликогена, то избыток углеводов превращается в жиры. Начальная последовательность реакций совпадает при этом с обычным окислительным путем, т.е. сначала из глюкозы образуется ацетил-КоА, но далее этот ацетил-КоА используется в цитоплазме клетки для синтеза длинноцепочечных жирных кислот. Процесс синтеза можно описать как обращение обычного процесса окисления жирных клеток. Затем жирные кислоты запасаются в виде нейтральных жиров (триглицеридов), отлагающихся в разных частях тела. Когда требуется энергия, нейтральные жиры подвергаются гидролизу и жирные кислоты поступают в кровь. Здесь они адсорбируются молекулами плазменных белков (альбуминов и глобулинов) и затем поглощаются клетками самых разных типов. Механизмов, способных осуществлять синтез глюкозы из жирных кислот, у животных нет, но у растений такие механизмы имеются.
Здесь они адсорбируются молекулами плазменных белков (альбуминов и глобулинов) и затем поглощаются клетками самых разных типов. Механизмов, способных осуществлять синтез глюкозы из жирных кислот, у животных нет, но у растений такие механизмы имеются.
Метаболизм липидов.
Липиды попадают в организм главным образом в форме триглицеридов жирных кислот. В кишечнике под действием ферментов поджелудочной железы они подвергаются гидролизу, продукты которого всасываются клетками стенки кишечника. Здесь из них вновь синтезируются нейтральные жиры, которые через лимфатическую систему поступают в кровь и либо транспортируются в печень, либо отлагаются в жировой ткани. Выше уже указывалось, что жирные кислоты могут также синтезироваться заново из углеводных предшественников. Следует отметить, что, хотя в клетках млекопитающих может происходить включение одной двойной связи в молекулы длинноцепочечных жирных кислот (между С–9 и С–10), включать вторую и третью двойную связь эти клетки неспособны. Поскольку жирные кислоты с двумя и тремя двойными связями играют важную роль в метаболизме млекопитающих, они в сущности являются витаминами. Поэтому линолевую (C18:2) и линоленовую (C18:3) кислоты называют незаменимыми жирными кислотами. В то же время в клетках млекопитающих в линоленовую кислоту может включаться четвертая двойная связь и путем удлинения углеродной цепи может образоваться арахидоновая кислота (C20:4), также необходимый участник метаболических процессов.
Поскольку жирные кислоты с двумя и тремя двойными связями играют важную роль в метаболизме млекопитающих, они в сущности являются витаминами. Поэтому линолевую (C18:2) и линоленовую (C18:3) кислоты называют незаменимыми жирными кислотами. В то же время в клетках млекопитающих в линоленовую кислоту может включаться четвертая двойная связь и путем удлинения углеродной цепи может образоваться арахидоновая кислота (C20:4), также необходимый участник метаболических процессов.
В процессе синтеза липидов остатки жирных кислот, связанные с коферментом А (ацил-КоА), переносятся на глицерофосфат – эфир фосфорной кислоты и глицерина. В результате образуется фосфатидная кислота – соединение, в котором одна гидроксильная группа глицерина этерифицирована фосфорной кислотой, а две группы – жирными кислотами. При образовании нейтральных жиров фосфорная кислота удаляется путем гидролиза, и ее место занимает третья жирная кислота в результате реакции с ацил-КоА. Кофермент А образуется из пантотеновой кислоты (одного из витаминов). В его молекуле имеется сульфгидрильная (– SH) группа, способная реагировать с кислотами с образованием тиоэфиров. При образовании фосфолипидов фосфатидная кислота реагирует непосредственно с активированным производным одного из азотистых оснований, таких, как холин, этаноламин или серин.
В его молекуле имеется сульфгидрильная (– SH) группа, способная реагировать с кислотами с образованием тиоэфиров. При образовании фосфолипидов фосфатидная кислота реагирует непосредственно с активированным производным одного из азотистых оснований, таких, как холин, этаноламин или серин.
За исключением витамина D, все встречающиеся в организме животных стероиды (производные сложных спиртов) легко синтезируются самим организмом. Сюда относятся холестерин (холестерол), желчные кислоты, мужские и женские половые гормоны и гормоны надпочечников. В каждом случае исходным материалом для синтеза служит ацетил-КоА: из ацетильных групп путем многократно повторяющейся конденсации строится углеродный скелет синтезируемого соединения.
МЕТАБОЛИЗМ БЕЛКОВ
Синтез аминокислот.
Растения и большинство микроорганизмов могут жить и расти в среде, в которой для их питания имеются только минеральные вещества, диоксид углерода и вода. Это значит, что все обнаруживаемые в них органические вещества эти организмы синтезируют сами. Встречающиеся во всех живых клетках белки построены из 21 вида аминокислот, соединенных в различной последовательности. Аминокислоты синтезируются живыми организмами. В каждом случае ряд химических реакций приводит к образованию a-кетокислоты. Одна такая a-кетокислота, а именно a-кетоглутаровая (обычный компонент цикла трикарбоновых кислот), участвует в связывании азота по следующему уравнению:
Встречающиеся во всех живых клетках белки построены из 21 вида аминокислот, соединенных в различной последовательности. Аминокислоты синтезируются живыми организмами. В каждом случае ряд химических реакций приводит к образованию a-кетокислоты. Одна такая a-кетокислота, а именно a-кетоглутаровая (обычный компонент цикла трикарбоновых кислот), участвует в связывании азота по следующему уравнению:
a-Кетоглутаровая кислота + NH3 + НАДЧН ®
® Глутаминовая кислота + НАД.
Азот глутаминовой кислоты может быть затем передан любой из других a-кетокислот с образованием соответствующей аминокислоты.
Организм человека и большинства других животных сохранил способность синтезировать все аминокислоты за исключением девяти т.н. незаменимых аминокислот. Поскольку кетокислоты, соответствующие этим девяти, не синтезируются, незаменимые аминокислоты должны поступать с пищей.
Синтез белков.
Аминокислоты нужны для биосинтеза белка. Процесс биосинтеза протекает обычно следующим образом. В цитоплазме клетки каждая аминокислота «активируется» в реакции с АТФ, а затем присоединяется к концевой группе молекулы рибонуклеиновой кислоты, специфичной именно для данной аминокислоты. Эта сложная молекула связывается с небольшим тельцем, т.н. рибосомой, в положении, определяемом более длинной молекулой рибонуклеиновой кислоты, прикрепленной к рибосоме. После того как все эти сложные молекулы соответствующим образом выстроились, связи между исходной аминокислотой и рибонуклеиновой кислотой разрываются и возникают связи между соседними аминокислотами – синтезируется специфичный белок. Процесс биосинтеза поставляет белки не только для роста организма или для секреции в среду. Все белки живых клеток со временем претерпевают распад до составляющих их аминокислот, и для поддержания жизни клетки должны синтезироваться вновь.
Процесс биосинтеза протекает обычно следующим образом. В цитоплазме клетки каждая аминокислота «активируется» в реакции с АТФ, а затем присоединяется к концевой группе молекулы рибонуклеиновой кислоты, специфичной именно для данной аминокислоты. Эта сложная молекула связывается с небольшим тельцем, т.н. рибосомой, в положении, определяемом более длинной молекулой рибонуклеиновой кислоты, прикрепленной к рибосоме. После того как все эти сложные молекулы соответствующим образом выстроились, связи между исходной аминокислотой и рибонуклеиновой кислотой разрываются и возникают связи между соседними аминокислотами – синтезируется специфичный белок. Процесс биосинтеза поставляет белки не только для роста организма или для секреции в среду. Все белки живых клеток со временем претерпевают распад до составляющих их аминокислот, и для поддержания жизни клетки должны синтезироваться вновь.
Синтез других азотсодержащих соединений.
В организме млекопитающих аминокислоты используются не только для биосинтеза белков, но и как исходный материал для синтеза многих азотсодержащих соединений. Аминокислота тирозин является предшественником гормонов адреналина и норадреналина. Простейшая аминокислота глицин служит исходным материалом для биосинтеза пуринов, входящих в состав нуклеиновых кислот, и порфиринов, входящих в состав цитохромов и гемоглобина. Аспарагиновая кислота – предшественник пиримидинов нуклеиновых кислот. Метильная группа метионина передается ряду других соединений в ходе биосинтеза креатина, холина и саркозина. При биосинтезе креатина от одного соединения к другому передается также и гуанидиновая группировка аргинина. Триптофан служит предшественником никотиновой кислоты, а из валина в растениях синтезируется такой витамин, как пантотеновая кислота. Все это лишь отдельные примеры использования аминокислот в процессах биосинтеза.
Аминокислота тирозин является предшественником гормонов адреналина и норадреналина. Простейшая аминокислота глицин служит исходным материалом для биосинтеза пуринов, входящих в состав нуклеиновых кислот, и порфиринов, входящих в состав цитохромов и гемоглобина. Аспарагиновая кислота – предшественник пиримидинов нуклеиновых кислот. Метильная группа метионина передается ряду других соединений в ходе биосинтеза креатина, холина и саркозина. При биосинтезе креатина от одного соединения к другому передается также и гуанидиновая группировка аргинина. Триптофан служит предшественником никотиновой кислоты, а из валина в растениях синтезируется такой витамин, как пантотеновая кислота. Все это лишь отдельные примеры использования аминокислот в процессах биосинтеза.
Азот, поглощаемый микроорганизмами и высшими растениями в виде иона аммония, расходуется почти целиком на образование аминокислот, из которых затем синтезируются многие азотсодержащие соединения живых клеток. Избыточных количеств азота ни растения, ни микроорганизмы не поглощают. В отличие от них, у животных количество поглощенного азота зависит от содержащихся в пище белков. Весь азот, поступивший в организм в виде аминокислот и не израсходованный в процессах биосинтеза, довольно быстро выводится из организма с мочой. Происходит это следующим образом. В печени неиспользованные аминокислоты передают свой азот a-кетоглутаровой кислоте с образованием глутаминовой кислоты, которая дезаминируется, высвобождая аммиак. Далее азот аммиака может либо на время запасаться путем синтеза глутамина, либо сразу же использоваться для синтеза мочевины, протекающего в печени.
В отличие от них, у животных количество поглощенного азота зависит от содержащихся в пище белков. Весь азот, поступивший в организм в виде аминокислот и не израсходованный в процессах биосинтеза, довольно быстро выводится из организма с мочой. Происходит это следующим образом. В печени неиспользованные аминокислоты передают свой азот a-кетоглутаровой кислоте с образованием глутаминовой кислоты, которая дезаминируется, высвобождая аммиак. Далее азот аммиака может либо на время запасаться путем синтеза глутамина, либо сразу же использоваться для синтеза мочевины, протекающего в печени.
У глутамина есть и другая роль. Он может подвергаться гидролизу в почках с высвобождением аммиака, который поступает в мочу в обмен на ионы натрия. Этот процесс крайне важен как средство поддержания кислотно-щелочного равновесия в организме животного. Почти весь аммиак, происходящий из аминокислот и, возможно, из других источников, превращается в печени в мочевину, так что свободного аммиака в крови обычно почти нет. Однако при некоторых условиях довольно значительные количества аммиака содержит моча. Этот аммиак образуется в почках из глутамина и переходит в мочу в обмен на ионы натрия, которые таким образом реадсорбируются и задерживаются в организме. Этот процесс усиливается при развитии ацидоза – состояния, при котором организм нуждается в дополнительных количествах катионов натрия для связывания избытка ионов бикарбоната в крови.
Однако при некоторых условиях довольно значительные количества аммиака содержит моча. Этот аммиак образуется в почках из глутамина и переходит в мочу в обмен на ионы натрия, которые таким образом реадсорбируются и задерживаются в организме. Этот процесс усиливается при развитии ацидоза – состояния, при котором организм нуждается в дополнительных количествах катионов натрия для связывания избытка ионов бикарбоната в крови.
Избыточные количества пиримидинов тоже распадаются в печени через ряд реакций, в которых высвобождается аммиак. Что касается пуринов, то их избыток подвергается окислению с образованием мочевой кислоты, выделяющейся с мочой у человека и других приматов, но не у остальных млекопитающих. У птиц отсутствует механизм синтеза мочевины, и именно мочевая кислота, а не мочевина, является у них конечным продуктом обмена всех азотсодержащих соединений.
Нуклеиновые кислоты.
Структура и синтез этих азотсодержащих соединений подробно описаны в статье НУКЛЕИНОВЫЕ КИСЛОТЫ.
ОБЩИЕ ПРЕДСТАВЛЕНИЯ О МЕТАБОЛИЗМЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Можно сформулировать некоторые общие понятия, или «правила», касающиеся метаболизма. Приведенные ниже несколько главных «правил» позволяют лучше понять, как протекает и регулируется метаболизм.
1. Метаболические пути необратимы. Распад никогда не идет по пути, который являлся бы простым обращением реакций синтеза. В нем участвуют другие ферменты и другие промежуточные продукты. Нередко противоположно направленные процессы протекают в разных отсеках клетки. Так, жирные кислоты синтезируются в цитоплазме при участии одного набора ферментов, а окисляются в митохондриях при участии совсем другого набора.
2. Ферментов в живых клетках достаточно для того, чтобы все известные метаболические реакции могли протекать гораздо быстрее, чем это обычно наблюдается в организме. Следовательно, в клетках существуют какие-то регуляторные механизмы. Открыты разные типы таких механизмов.
а) Фактором, ограничивающим скорость метаболических превращений данного вещества, может быть поступление этого вещества в клетку; именно на этот процесс в таком случае и направлена регуляция. Роль инсулина, например, связана с тем, что он, по-видимому, облегчает проникновение глюкозы во все клетки, глюкоза же подвергается превращениям с той скоростью, с какой она поступает. Сходным образом проникновение железа и кальция из кишечника в кровь зависит от процессов, скорость которых регулируется.
Роль инсулина, например, связана с тем, что он, по-видимому, облегчает проникновение глюкозы во все клетки, глюкоза же подвергается превращениям с той скоростью, с какой она поступает. Сходным образом проникновение железа и кальция из кишечника в кровь зависит от процессов, скорость которых регулируется.
б) Вещества далеко не всегда могут свободно переходить из одного клеточного отсека в другой; есть данные, что внутриклеточный перенос регулируется некоторыми стероидными гормонами.
в) Выявлено два типа сервомеханизмов «отрицательной обратной связи».
У бактерий были обнаружены примеры того, что присутствие продукта какой-нибудь последовательности реакций, например аминокислоты, подавляет биосинтез одного из ферментов, необходимых для образования этой аминокислоты.
В каждом случае фермент, биосинтез которого оказывается затронутым, был ответствен за первый «определяющий» этап (на схеме реакция 4) метаболического пути, ведущего к синтезу данной аминокислоты.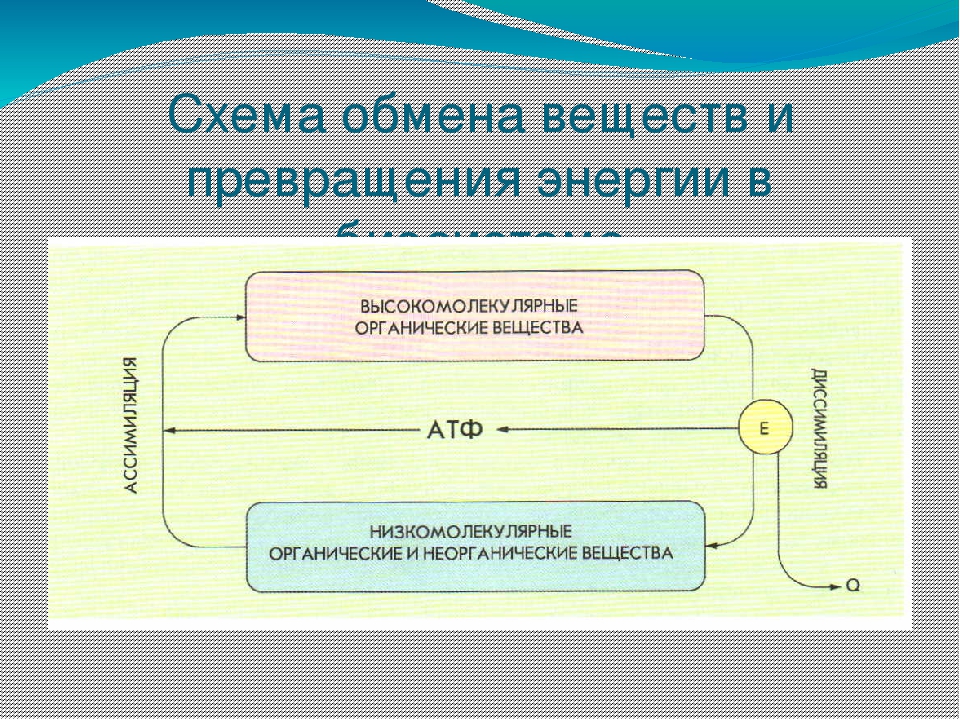
Второй механизм хорошо изучен у млекопитающих. Это простое ингибирование конечным продуктом (в нашем случае – аминокислотой) фермента, ответственного за первый «определяющий» этап метаболического пути.
Еще один тип регулирования посредством обратной связи действует в тех случаях, когда окисление промежуточных продуктов цикла трикарбоновых кислот сопряжено с образованием АТФ из АДФ и фосфата в процессе окислительного фосфорилирования. Если весь имеющийся в клетке запас фосфата и (или) АДФ уже исчерпан, то окисление приостанавливается и может возобновиться лишь после того, как этот запас вновь станет достаточным. Таким образом, окисление, смысл которого в том, чтобы поставлять полезную энергию в форме АТФ, происходит только тогда, когда возможен синтез АТФ.
3. В биосинтетических процессах участвует сравнительно небольшое число строительных блоков, каждый из которых используется для синтеза многих соединений. Среди них можно назвать ацетилкофермент А, глицерофосфат, глицин, карбамилфосфат, поставляющий карбамильную (H2N–CO–) группу, производные фолиевой кислоты, служащие источником гидроксиметильной и формильной групп, S-аденозилметионин – источник метильных групп, глутаминовую и аспарагиновую кислоты, поставляющие аминогруппы, и наконец, глутамин – источник амидных групп. Из этого относительно небольшого числа компонентов строятся все те разнообразные соединения, которые мы находим в живых организмах.
Из этого относительно небольшого числа компонентов строятся все те разнообразные соединения, которые мы находим в живых организмах.
4. Простые органические соединения редко участвуют в метаболических реакциях непосредственно. Обычно они должны быть сначала «активированы» путем присоединения к одному из ряда соединений, универсально используемых в метаболизме. Глюкоза, например, может подвергнуться окислению лишь после того, как она будет этерифицирована фосфорной кислотой, для прочих же своих превращений она должна быть этерифицирована уридиндифосфатом. Жирные кислоты не могут быть вовлечены в метаболические превращения прежде, чем они образуют эфиры с коферментом А. Каждый из этих активаторов либо родствен одному из нуклеотидов, входящих в состав рибонуклеиновой кислоты, либо образуется из какого-нибудь витамина. Легко понять в связи с этим, почему витамины требуются в таких небольших количествах. Они расходуются на образование «коферментов», а каждая молекула кофермента на протяжении жизни организма используется многократно, в отличие от основных питательных веществ (например, глюкозы), каждая молекула которых используется только один раз.
В заключение следует сказать, что термин «метаболизм», означавший ранее нечто не более сложное, чем просто использование углеводов и жиров в организме, теперь применяется для обозначения тысяч ферментативных реакций, вся совокупность которых может быть представлена как огромная сеть метаболических путей, многократно пересекающихся (из-за наличия общих промежуточных продуктов) и управляемых очень тонкими регуляторными механизмами.
МЕТАБОЛИЗМ МИНЕРАЛЬНЫХ ВЕЩЕСТВ
Относительное содержание.
Различные элементы, встречающиеся в живых организмах, перечислены ниже в убывающем порядке в зависимости от их относительного содержания: 1) кислород, углерод, водород и азот; 2) кальций, фосфор, калий и сера; 3) натрий, хлор, магний и железо; 4) марганец, медь, молибден, селен, йод и цинк; 5) алюминий, фтор, кремний и литий; 6) бром, мышьяк, свинец и, возможно, некоторые другие.
Кислород, углерод, водород и азот – это те элементы, из которых построены мягкие ткани тела. Они входят в состав таких соединений, как углеводы, липиды, белки, вода, диоксид углерода и аммиак. Элементы, перечисленные в пп. 2 и 3, находятся в организме обычно в виде одного или нескольких неорганических соединений, а элементы пп. 4, 5 и 6 присутствуют только в следовых количествах и потому их называют микроэлементами.
Они входят в состав таких соединений, как углеводы, липиды, белки, вода, диоксид углерода и аммиак. Элементы, перечисленные в пп. 2 и 3, находятся в организме обычно в виде одного или нескольких неорганических соединений, а элементы пп. 4, 5 и 6 присутствуют только в следовых количествах и потому их называют микроэлементами.
Распределение в организме.
Кальций.
Кальций присутствует главным образом в костной ткани и в зубах, преимущественно в виде фосфата и в небольших количествах в виде карбоната и фторида. Поступающий с пищей кальций всасывается в основном в верхних отделах кишечника, имеющих слабокислую реакцию. Этому всасыванию (у человека здесь всасывается всего 20–30% кальция пищи) способствует витамин D. Под действием витамина D клетки кишечника вырабатывают особый белок, который связывает кальций и облегчает его перенос через стенку кишечника в кровь. На всасывание влияет также присутствие некоторых других веществ, в особенности фосфата и оксалата, которые в малых количествах способствуют всасыванию, а в больших, наоборот, подавляют его.
В крови около половины кальция связано с белком, остальное составляют ионы кальция. Соотношение ионизированной и неионизированной форм зависит от общей концентрации кальция в крови, а также от содержания белка и фосфата и концентрации водородных ионов (рН крови). Доля неионизированного кальция, на которую влияет уровень белка, позволяет косвенным образом судить о качестве питания и об эффективности работы печени, в которой идет синтез плазменных белков.
На количество ионизированного кальция влияют, с одной стороны, витамин D и факторы, воздействующие на всасывание, а с другой – паратиреоидный гормон и, возможно, также витамин D, поскольку оба эти вещества регулируют как скорость отложения кальция в костной ткани, так и его мобилизацию, т.е. вымывание из костей. Избыток паратиреоидного гормона стимулирует выход кальция из костной ткани, что приводит к повышению его концентрации в плазме. Изменяя скорости всасывания и экскреции кальция и фосфата, а также скорости образования костной ткани и ее разрушения, эти механизмы строго контролируют концентрацию кальция и фосфата в сыворотке крови. Ионы кальция играют регулирующую роль во многих физиологических процессах, в том числе в нервных реакциях, мышечном сокращении, свертывании крови. Выведение кальция из организма происходит в норме в основном (на 2/3) через желчь и кишечник и в меньшей степени (1/3) – через почки.
Ионы кальция играют регулирующую роль во многих физиологических процессах, в том числе в нервных реакциях, мышечном сокращении, свертывании крови. Выведение кальция из организма происходит в норме в основном (на 2/3) через желчь и кишечник и в меньшей степени (1/3) – через почки.
Фосфор.
Метаболизм фосфора – одного из главных компонентов костной ткани и зубов – во многом зависит от тех же факторов, что и метаболизм кальция. Фосфор в виде фосфата присутствует в организме также в сотнях различных физиологически важных органических эфиров. Паратиреоидный гормон стимулирует выведение фосфора с мочой и выход его из костной ткани; тем самым он регулирует концентрацию фосфора в плазме крови.
Натрий.
Натрий – главный катион внеклеточной жидкости – вместе с белком, хлоридом и бикарбонатом играет важнейшую роль в регулировании осмотического давления и pH (концентрации водородных ионов) крови. В клетках, напротив, содержится очень мало натрия, так как они обладают механизмом для выведения ионов натрия и удержания ионов калия. Весь натрий, превышающий потребности организма, очень быстро выводится через почки.
Весь натрий, превышающий потребности организма, очень быстро выводится через почки.
Поскольку во всех процессах выделения натрий теряется, он должен постоянно поступать в организм с пищей. При ацидозе, когда необходимо, чтобы из организма выводились большие количества анионов (например, хлорида или ацетоацетата), почки предотвращают чрезмерную потерю натрия благодаря образованию аммиака из глутамина. Выведение натрия через почки регулируется гормоном коры надпочечников альдостероном. Под действием этого гормона в кровь возвращается достаточно натрия для поддержания нормального осмотического давления и нормального объема внеклеточной жидкости.
Суточная потребность в хлористом натрии составляет 5–10 г. Эта величина возрастает при поглощении больших количеств жидкости, когда усиливается потоотделение и выделяется больше мочи.
Калий.
В отличие от натрия, калий содержится в клетках в больших количествах, но во внеклеточной жидкости его мало. Главная функция калия – регулирование внутриклеточного осмотического давления и поддержание кислотно-щелочного равновесия. Он также играет важную роль в проведении нервного импульса и во многих ферментных системах, в том числе и в тех, которые участвуют в мышечном сокращении. Калий широко распространен в природе, и его много в любой пище, так что спонтанно калиевая недостаточность возникнуть не может. В плазме концентрация калия регулируется альдостероном, стимулирующим его экскрецию с мочой.
Он также играет важную роль в проведении нервного импульса и во многих ферментных системах, в том числе и в тех, которые участвуют в мышечном сокращении. Калий широко распространен в природе, и его много в любой пище, так что спонтанно калиевая недостаточность возникнуть не может. В плазме концентрация калия регулируется альдостероном, стимулирующим его экскрецию с мочой.
Сера.
С пищей сера поступает в организм главным образом в составе двух аминокислот – цистина и метионина. На конечных этапах метаболизма этих аминокислот сера высвобождается и в результате окисления переводится в неорганическую форму. В составе цистина и метионина сера присутствует в структурных белках. Важную роль играет также сульфгидрильная (–SH) группа цистеина, от которой зависит активность многих ферментов.
Большая часть серы выводится с мочой в виде сульфата. Небольшое количество экскретируемого сульфата обычно связано с органическими соединениями типа фенолов.
Магний.
Метаболизм магния сходен с метаболизмом кальция, и в виде комплекса с фосфатом этот элемент тоже входит в состав костной ткани. Магний присутствует во всех живых клетках, где он функционирует как необходимый компонент многих ферментных систем; эта его роль была убедительно продемонстрирована на примере углеводного обмена в мышцах. Магний, как и калий, широко распространен, и вероятность возникновения его недостаточности очень мала.
Магний присутствует во всех живых клетках, где он функционирует как необходимый компонент многих ферментных систем; эта его роль была убедительно продемонстрирована на примере углеводного обмена в мышцах. Магний, как и калий, широко распространен, и вероятность возникновения его недостаточности очень мала.
Железо.
Железо входит в состав гемоглобина и других гемопротеинов, а именно миоглобина (мышечного гемоглобина), цитохромов (дыхательных ферментов) и каталазы, а также в состав некоторых ферментов, не содержащих гемогруппы. Всасывается железо в верхних отделах кишечника, причем это единственный элемент, всасывающийся только тогда, когда его запас в организме полностью исчерпан. В плазме железо транспортируется в соединении с белком (трансферрином). Через почки железо не выводится; избыток его накапливается в печени в соединении с особым белком (ферритином).
Микроэлементы.
У каждого микроэлемента, присутствующего в организме, своя особая функция, связанная с тем, что он стимулирует действие того или иного фермента или как-либо иначе на него влияет. Цинк необходим для кристаллизации инсулина; кроме того, он является компонентом карбоангидразы (фермента, участвующего в транспорте диоксида углерода) и некоторых других ферментов. Молибден и медь – тоже необходимые компоненты различных ферментов. Иод требуется для синтеза трииодтиронина, гормона щитовидной железы. Фтор (входящий в состав зубной эмали) способствует предотвращению кариеса.
Цинк необходим для кристаллизации инсулина; кроме того, он является компонентом карбоангидразы (фермента, участвующего в транспорте диоксида углерода) и некоторых других ферментов. Молибден и медь – тоже необходимые компоненты различных ферментов. Иод требуется для синтеза трииодтиронина, гормона щитовидной железы. Фтор (входящий в состав зубной эмали) способствует предотвращению кариеса.
ИСПОЛЬЗОВАНИЕ МЕТАБОЛИТОВ
Углеводы.
Всасывание.
Моносахариды, или простые сахара, высвобождающиеся при переваривании углеводов пищи, переходят из кишечника в кровоток в результате процесса, называемого всасыванием. Механизм всасывания представляет собой сочетание простой диффузии и химической реакции (активного всасывания). Одна из гипотез, касающихся природы химической фазы процесса, предполагает, что в этой фазе моносахариды соединяются с фосфорной кислотой в реакции, катализируемой ферментом из группы киназ, после чего проникают в кровеносные сосуды и здесь высвобождаются в результате ферментативного дефосфорилирования (разрыва фосфатной связи), катализируемого одной из фосфатаз. Именно активным всасыванием объясняется то, что разные моносахариды всасываются с разной скоростью и что углеводы всасываются даже тогда, когда уровень сахара в крови выше, чем в кишечнике, т.е. в условиях, когда естественно было бы ожидать их перемещения в обратном направлении – из крови в кишечник.
Именно активным всасыванием объясняется то, что разные моносахариды всасываются с разной скоростью и что углеводы всасываются даже тогда, когда уровень сахара в крови выше, чем в кишечнике, т.е. в условиях, когда естественно было бы ожидать их перемещения в обратном направлении – из крови в кишечник.
Механизмы гомеостаза.
Поступающие в кровоток моносахариды повышают уровень сахара в крови. При голодании концентрация глюкозы в крови колеблется обычно от 70 до 100 мг на 100 мл крови. Этот уровень поддерживается с помощью механизмов, называемых механизмами гомеостаза (самостабилизации). Как только уровень сахара в крови в результате всасывания из кишечника повышается, в действие вступают процессы, выводящие сахар из крови, так что уровень его колеблется не слишком сильно.
Подобно глюкозе, все прочие моносахариды поступают из кровотока в печень, где превращаются в глюкозу. Теперь они неотличимы как от глюкозы, которая всосалась, так и от той, что уже была в организме, и подвергаются тем же метаболическим превращениям. Один из механизмов гомеостаза углеводов, функционирующий в печени, – это гликогенез, посредством которого глюкоза переходит из крови в клетки, где превращается в гликоген. Гликоген хранится в печени до тех пор, пока не произойдет снижение уровня сахара в крови: в этой ситуации гомеостатический механизм вызовет распад накопленного гликогена до глюкозы, которая вновь поступит в кровь.
Один из механизмов гомеостаза углеводов, функционирующий в печени, – это гликогенез, посредством которого глюкоза переходит из крови в клетки, где превращается в гликоген. Гликоген хранится в печени до тех пор, пока не произойдет снижение уровня сахара в крови: в этой ситуации гомеостатический механизм вызовет распад накопленного гликогена до глюкозы, которая вновь поступит в кровь.
Превращения и использование.
Поскольку кровь поставляет глюкозу во все ткани тела и все ткани используют ее для получения энергии, уровень глюкозы в крови снижается главным образом за счет ее использования.
В мышцах глюкоза крови превращается в гликоген. Однако мышечный гликоген не может быть использован для получения глюкозы, которая перешла бы в кровь. В нем заключен запас энергии, и скорость его использования зависит от мышечной активности. В мышечной ткани содержатся два соединения с большим запасом легко доступной энергии в форме богатых энергией фосфатных связей – креатинфосфат и аденозинтрифосфат (АТФ). При отщеплении от этих соединений их фосфатных групп высвобождается энергия для мышечного сокращения. Чтобы мышца вновь могла сокращаться, эти соединения должны быть восстановлены в своей исходной форме. Для этого требуется энергия, которую поставляет окисление продуктов распада гликогена. При мышечном сокращении гликоген превращается в глюкозофосфат, а затем – через ряд реакций – во фруктозодифосфат. Фруктозодифосфат распадается на два трехуглеродных соединения, из которых после ряда этапов образуется сначала пировиноградная кислота, а в конечном итоге – молочная кислота, как об этом уже говорилось при описании метаболизма углеводов. Это превращение гликогена в молочную кислоту, сопровождающееся высвобождением энергии, может происходить в отсутствие кислорода.
При отщеплении от этих соединений их фосфатных групп высвобождается энергия для мышечного сокращения. Чтобы мышца вновь могла сокращаться, эти соединения должны быть восстановлены в своей исходной форме. Для этого требуется энергия, которую поставляет окисление продуктов распада гликогена. При мышечном сокращении гликоген превращается в глюкозофосфат, а затем – через ряд реакций – во фруктозодифосфат. Фруктозодифосфат распадается на два трехуглеродных соединения, из которых после ряда этапов образуется сначала пировиноградная кислота, а в конечном итоге – молочная кислота, как об этом уже говорилось при описании метаболизма углеводов. Это превращение гликогена в молочную кислоту, сопровождающееся высвобождением энергии, может происходить в отсутствие кислорода.
При недостатке кислорода молочная кислота накапливается в мышцах, диффундирует в кровоток и поступает в печень, где из нее вновь образуется гликоген. Если кислорода достаточно, то молочная кислота в мышцах не накапливается. Вместо этого она, как это описано выше, полностью окисляется через цикл трикарбоновых кислот до диоксида углерода и воды с образованием АТФ, который может быть использован для сокращения.
Вместо этого она, как это описано выше, полностью окисляется через цикл трикарбоновых кислот до диоксида углерода и воды с образованием АТФ, который может быть использован для сокращения.
Метаболизм углеводов в нервной ткани и эритроцитах отличается от метаболизма в мышцах тем, что гликоген здесь не участвует. Однако и здесь промежуточными продуктами являются пировиноградная и молочная кислоты, образующиеся при расщеплении глюкозофосфата.
Глюкоза используется не только в клеточном дыхании, но и во многих других процессах: синтезе лактозы (молочного сахара), образовании жиров, а также особых сахаров, входящих в состав полисахаридов соединительной ткани и ряда других тканей.
Гликоген печени, синтезируемый при всасывании углеводов в кишечнике, служит самым доступным источником глюкозы, когда всасывание отсутствует. Если этот источник оказывается исчерпанным, в печени начинается процесс глюконеогенеза. Глюкоза образуется при этом из некоторых аминокислот (из 100 г белка образуется 58 г глюкозы) и нескольких других неуглеводных соединений, в том числе из глицериновых остатков нейтральных жиров.
Некоторую, хотя и не столь важную, роль в метаболизме углеводов играют почки. Они выводят из организма избыток глюкозы, когда ее концентрация в крови слишком высока; при меньших концентрациях глюкоза практически не выводится.
В регулировании метаболизма углеводов участвует несколько гормонов, в том числе гормоны поджелудочной железы, передней доли гипофиза и коры надпочечников.
Гормон поджелудочной железы инсулин снижает концентрацию глюкозы в крови и повышает ее концентрацию в клетках. По-видимому, он стимулирует также и запасание гликогена в печени. Кортикостерон, гормон коры надпочечников, и адреналин, вырабатываемый мозговым веществом надпочечников, воздействуют на метаболизм углеводов, стимулируя распад гликогена (главным образом в мышцах и печени) и синтез глюкозы (в печени).
Липиды.
Всасывание.
В кишечнике после переваривания жиров остаются главным образом свободные жирные кислоты с небольшой примесью холестерина и лецитина и следами жирорастворимых витаминов. Все эти вещества очень тонко диспергированы благодаря эмульгирующему и солюбилизирующему действию солей желчных кислот. Солюбилизирующее действие обычно связывают с образованием нестойких химических соединений между жирными кислотами и солями желчных кислот. Эти комплексы проникают в клетки эпителия тонкого кишечника и здесь распадаются на жирные кислоты и соли желчных кислот. Последние переносятся в печень и вновь секретируются с желчью, а жирные кислоты вступают в соединение с глицерином или холестерином. Образовавшиеся реконструированные жиры поступают в лимфатические сосуды брыжейки в форме млечного сока, т.н. «хилуса». Из сосудов брыжейки хилус по лимфатической системе через грудной проток поступает в кровеносную систему.
После переваривания пищи содержание липидов в крови возрастает приблизительно от 500 мг (уровень при голодании) до 1000 мг на 100 мл плазмы. Присутствующие в крови липиды представляют собой смесь жирных кислот, нейтральных жиров, фосфолипидов (лецитина и кефалина), холестерина и эфиров холестерина.
Распределение.
Кровь доставляет липиды в разные ткани тела и прежде всего в печень. Печень обладает способностью модифицировать поступающие в нее жирные кислоты. Это особенно выражено у видов, запасающих жиры с высоким содержанием насыщенных или, наоборот, ненасыщенных жирных кислот: в печени этих животных соотношение насыщенных и ненасыщенных кислот изменяется таким образом, что отлагающийся жир по своему составу соответствует жиру, свойственному данному организму.
Жиры в печени либо используются для получения энергии, либо переходят в кровь и доставляются ею в разные ткани. Здесь они могут включаться в структурные элементы тканей, но большая их часть отлагается в жировых депо, где они хранятся до тех пор, пока не возникнет потребность в энергии; тогда они снова переносятся в печень и подвергаются здесь окислению.
Метаболизм липидов, как и углеводов, регулируется гомеостатически. Механизмы гомеостаза, воздействующие на липидный и углеводный обмен, видимо, тесно связаны, поскольку при замедлении метаболизма углеводов усиливается метаболизм липидов, и наоборот.
Превращения и использование.
Четырехуглеродные кислоты – ацетоуксусная (продукт конденсации двух ацетатных единиц) и b-гидроксимасляная – и трехуглеродное соединение ацетон, образующийся при отщеплении одного атома углерода от ацетоуксусной кислоты, известны под общим названием кетоновых (ацетоновых) тел. В норме кетоновые тела присутствуют в крови в небольших количествах. Избыточное их образование при тяжелом диабете ведет к повышению их содержания в крови (кетонемия) и в моче (кетонурия) – это состояние обозначают термином «кетоз».
Белки.
Всасывание.
При переваривании белков пищеварительными ферментами образуется смесь из аминокислот и небольших пептидов, содержащих от двух до десяти остатков аминокислот. Эти продукты всасываются слизистой кишечника, и здесь гидролиз завершается – пептиды также распадаются до аминокислот. Поступившие в кровь аминокислоты смешиваются с находящимися здесь такими же аминокислотами. В крови содержится смесь из аминокислот, поступивших из кишечника, образовавшихся при распаде тканевых белков и синтезированных организмом заново.
Синтез.
В тканях непрерывно идет распад белков и их новообразование. Содержащиеся в крови аминокислоты избирательно поглощаются тканями как исходный материал для построения белков, а из тканей в кровь поступают другие аминокислоты. Синтезу и распаду подвергаются не только структурные белки, но и белки плазмы крови, а также белковые гормоны и ферменты.
Во взрослом организме аминокислоты или белки практически не запасаются, поэтому удаление аминокислот из крови происходит с такой же скоростью, как и их поступление из тканей в кровь. В растущем организме формируются новые ткани, и на этот процесс расходуется больше аминокислот, чем поступает в кровь за счет распада тканевых белков.
Печень участвует в метаболизме белков самым активным образом. Здесь синтезируются белки плазмы крови – альбумины и глобулины – а также собственные ферменты печени. Так, при потере плазменных белков содержание альбумина в плазме восстанавливается – за счет интенсивного синтеза – довольно быстро. Аминокислоты в печени используются не только для образования белков, но подвергаются также расщеплению, в ходе которого извлекается заключенная в них энергия.
Превращения и использование.
Если аминокислоты используются в качестве источника энергии, то отщепляемая от них аминогруппа (–NH2) направляется на образование мочевины, а не содержащий азота остаток молекулы окисляется приблизительно так же, как глюкоза или жирные кислоты.
Так называемый «орнитиновый цикл» описывает, как происходит превращение аммиака в мочевину. В этом цикле аминогруппа, отщепившаяся от аминокислоты в форме аммиака, присоединяется вместе с диоксидом углерода к молекуле орнитина с образованием цитруллина. Цитруллин присоединяет второй атом азота, на этот раз от аспарагиновой кислоты, и превращается в аргинин. Далее аргинин подвергается гидролизу с образованием мочевины и орнитина. Орнитин может теперь вновь вступить в цикл, а мочевина выводится из организма через почки как один из конечных продуктов метаболизма.
См. также ГОРМОНЫ; ФЕРМЕНТЫ; ЖИРЫ И МАСЛА; НУКЛЕИНОВЫЕ КИСЛОТЫ; БЕЛКИ; ВИТАМИНЫ.
ПЭТ-КТ | ядерная медицина
Большинство клеток в человеческом организме используют глюкозу в качестве «поставщика» энергии. Точно также происходит с опухолевыми клетками многочисленных раковых заболеваний. По сравнению с другими клетками у них отмечается повышенный обмен веществ, и они «потребляют» особенно много глюкозы.
ПЭТ
Данное обстоятельство мы используем в своих целях, когда, например, вводим пациентам слабую инъекцию радиоактивно маркированной глюкозы (ФДГ – фтордезоксиглюкоза). При помощи ПЭТ (позитронно-эмиссионная томография) мы видим слабо радиоактивные субстанции в обмене веществ, и, таким образом, можем отобразить биохимические и физиологические функции. Однако при помощи метода ПЭТ практически не отображается информация об анатомических аспектах организма.
КТ
По этой причине мы связываем метод ПЭТ с уже известной КТ (компьютерная томография). Она предоставляет нам топограммы («послойные» снимки) желаемых областей, поэтому ее еще называют «послойный рентген».
Комбинация двух методов
Когда мы проводим наших пациентов полностью в идентичном положении через детекторные кольца комбинированноого аппарата ПЭТ-КТ мы производим различные снимки тех же самых зон. Эти снимки мы можем рассматривать как по отдельности, так и комбинированно. В большинстве случаев снимок из компьютерного томографа изображается в оттенках серого цвета, а информация, полученная в ПЭТ – в цвете. Таким образом мы соотносим области с повышенным обменом глюкозы в точности до миллиметра.
ПЭТ-КТ в диагностике раковых заболеваний
Основная область применения ПЭТ – онкология. При помощи ПЭТ-КТ мы можем получить информацию о наличии злокачественной опухоли, распространении опухоли (стадирование), эффективности лечения (контроль терапии) или о повторном появлении опухоли (рецидив, ДД рубец, посттерапевтические изменения). Преимуществом ПЭТ-КТ является исследование всего тела, при помощи которого может быть произведена оценка как главной опухоли (первичная), так и метастазов в лимфоузлах и отдаленных метастазов. Кроме этого исследование ПЭТ-КТ может быть использовано в качестве планирования взятия ткани (биопсия), а также с целью планирования лучевой терапии опухолей.
ПЭТ-КТ для неврологических и кардиологических исследований
Другие области применения ПЭТ-КТ: неврология, например, в отношении вопроса по заболеванию Альцгеймера (дифференциальная диагностика деменции), кардиология, например, вопрос в отношении способности способности к восстановлению зон сердечной мышцы со сниженным кровотоком перед операцией по шунтированию или расширению сосудов (витальная диагностика), и медицина воспалительных заболеваний, например, при поиске очагов воспаления.
Применение ПЭТ-КТ у детей
ПЭТ-КТ также может применяться и при обследовании детей любого возраста. Начиная с 4 лет дети, в большинстве случаев, такие кооперативные (хорошо идут на контакт с врачом), что им даже не требуется прием успокоительного средства или снотворного. Более юные дети должны проходить обследование в то время, когда они уставшие или обычно спят (поздняя первая половина дня). После введения ФДГ ребенку дают успокоительное средство в качестве микроклизмы (свечка), которая поддерживает сон ребенка. Груднички могут получить молоко (смесь или материнское молоко) спустя полчаса после введения ФДГ, потом они, в большинстве случаев, самостоятельно засыпают. В течение всего времени подготовки и во время ПЭТ вы можете остаться со своим ребенком. Только в течение короткой фазы снимка КТ (30 секунд) вам следует покинуть помещение.
Врожденные заболевания обмена веществ | Сант Жоан де Деу
Что такое наследственные болезни обмена веществ (врожденные метаболические заболевания)
Патологии, также известные как врожденные нарушения метаболизма, — это заболевания, причина которых кроется в генетическом изменении белка или фермента, в результате чего блокируется определенный процесс метаболизма. Такая блокировка влияет на нормальное функционирование некоторых клеток и органов и проявляется рядом симптомов, различных у каждого пациента. Среди таких симптомов могут встречаться разные виды неврологических синдромов.
Эта группа патологий очень обширна, однако ее можно систематизировать с помощью действующей классификации, которая в данный момент претерпевает значительные изменения ввиду того, что сегодня мы располагаем гораздо большими знаниями о базовых механизмах развития таких патологий. Ниже приведены основные группы патологий, составленные на основании типа поражения организма при каждой из них.
Врожденное нарушение метаболизма малых молекул
Влияют на промежуточный метаболизм. Сюда входят аминоацидопатии (фенилкетонурия и пропионовая ацидурия). Также сюда входит нарушения обмена углеводов или нейромедиаторов и нейромодуляторов.
Врожденное нарушение энергетического обмена
Характеризуется недостаточной выработкой и использованием энергии. Сюда входят митохондриальные заболевания, недостаточная выработка пирувата или глюкозы (в мышцах или печени) и т. д.
Врожденное нарушение метаболизма сложных молекул
Группа заболеваний, которые препятствуют синтезу больших молекул. Они проявляются в виде постоянных симптомов, не связанных с питанием. Сюда входят лизосомные (мукополисахаридоз, олигосахаридоз, сфинголипидоз и т. д.), пероксисомальные (синдром Цельвегера, адренолейкодистрофия, сцепленная с хромосомой Х) заболевания и врожденные нарушения гликозилирования, а также другие врожденные нарушения метаболизма.
Роль нейротрансмиттеров в регуляции энергетического гомеостаза и возможности медикаментозной коррекции его нарушений при ожирении | Дедов
Ожирение во всем мире является одной из наиболее значимых проблем здравоохранения. ВОЗ определяет ожирение как хроническое заболевание, распространенное как в развитых, так и развивающихся странах и поражающее в равной степени детей и взрослых. Европейское медицинское агентство дает определение ожирению как хроническому заболеванию, вызываемому генетическими, метаболическими, поведенческими факторами и факторами окружающей среды и связанному с повышением частоты осложнений и смертностью.
По последним данным ВОЗ, в период с 1980 по 2013 гг. в мире отмечено увеличение доли взрослых, имеющих индекс массы тела (ИМТ) выше 25 кг/м2, с 28,8% до 36,9% у мужчин и с 29,8% до 38% у женщин.
В основе современного подхода к терапии ожирения лежит признание хронического характера заболевания, то есть невозможности его полного излечения, и, следовательно, необходимости долгосрочного лечения [1]. Нередко при ожирении отмечаются нарушения со стороны психики, у человека появляется непреодолимое желание потреблять пищу, причем в ряде случаев это не приносит ему удовольствия. Иногда даже при сознательном отношении к диетотерапии и достаточной мотивации уменьшение потребления пищи и изменение ее состава очень трудно переносится больным. В таких случаях показана фармакотерапия ожирения, в том числе препараты, влияющие на пищевое поведение.
Следует отметить, что в ряде случаев даже при проведении фармакотерапии ожирения препаратами, доказавшими свою эффективность, после прекращения лечения пациенты возвращаются к своим пищевым привычкам и пристрастиям. В этой связи актуальным продолжает оставаться поиск иных методик коррекции пищевого поведения. Известно, что активация алиментарных зон коры достигается путем предъявления различных стимулов – зрительных, обонятельных, вкусовых [2]. Уникальный вариант ответа головного мозга на пищу и связанные с ней стимулы могут помочь объяснить возбуждение аппетита в той или иной ситуации. Поисковые работы, направленные на определение функционально значимых зон коры с последующим индивидуальным картированием, представляются перспективными с точки зрения разработок новых методов и подходов к лечению ожирения [3].
Итак, количество пищи, которое человек съедает, определяется внутренней потребностью, называемой голодом. Вид пищи, которому субъект отдает предпочтение, обусловлен аппетитом. Эти ауторегуляторные механизмы чрезвычайно важны для адекватного снабжения организма питательными веществами. Однако функциональная организация гипоталамуса или прочих нервных центров, отвечающих за пищевое поведение у людей с ожирением, отличается от таковой у людей с отсутствием избыточной массы тела [4]. Это могут быть нарушения медиаторных или рецепторных механизмов, нейрональных путей гипоталамуса, регулирующих пищевое поведение. В пользу такой точки зрения свидетельствуют наблюдения за пациентами, которым удалось вернуться к нормальной массе тела на фоне диетотерапии и у которых при этом обычно формируется чувство голода более сильное, чем у обычных людей. Это означает, что регуляторные системы, контролирующие пищевое поведение, у людей с ожирением запрограммированы исходно на более высокий уровень запасания питательных веществ, чем у людей с нормальной массой тела.
Регуляция энергетического баланса осуществляется двумя типами нейронов аркуантных ядер [5].
- Проопиомеланокортиновыми нейронами (РОМС, ПОМК), которые выделяют альфа-меланоцитостимулирующий гормон (α-MSH, альфа-МСГ) и кокаин- и амфетамин-опосредованные транскрипты (САRT, КАРТ), уменьшающие потребление пищи и увеличивающие расход энергии.
- Нейронами, которые продуцируют меланин-опосредованный белок (AGRP, или агути-подобный пептид, АПП) и нейропептид Y (NPY, НПY), увеличивающие потребление пищи и уменьшающие расход энергии.
Альфа-меланоцитостимулирующий гормон, выделяемый РОМС-нейронами, стимулирует меланокортиновые рецепторы (МСR3 и МСR4) паравентрикулярных ядер, которые затем активируют нейрональный путь, проецирующийся на ядра солитарного тракта, и повышают симпатическую активность и расход энергии. Меланин-опосредованный белок действует как антагонист МСR4 [5].
Инсулин, лептин и холецистокинин (гормоны, ингибирующие AGPG- и NPY-нейроны и стимулирующие соседние РОМС- и САRT-нейроны) уменьшают потребление пищи [6]. Грелин активирует AGPG- и NPY-нейроны и стимулирует потребление пищи. Рецепторы растяжения желудка активируют сенсорные афферентные пути в составе блуждающего нерва и ингибируют потребление пищи. Пептид YY (PYY) и холецистокинин являются гастроинтестинальными гормонами, которые выделяются при пищеварении и подавляют дальнейшее потребление пищи. Грелин, выделяемый желудком, особенно во время голодания, стимулирует аппетит. Лептин-гормон, продуцируемый жировыми клетками в возрастающих количествах при увеличении их размеров, ингибирует потребление пищи.
Существует много химических посредников, влияющих на структуры гипоталамуса, которые вместе образуют центр координации пищевого поведения и насыщения [7]. Некоторые из них суммированы в таблице 1.
Таблица 1. Гормоны и нейромедиаторы, влияющие на гипоталамические центры голода и насыщения | |
анорексигенные | орексигенные |
Альфа-меланоцитостимулирующий гормон | Нейропептид Y |
Лептин | Меланин-опосредованный белок |
Серотонин | Меланин-концентрирующий гормон |
Норадреналин | Орексины А и В |
Кортикотропин-рилизинг-гормон | Эндорфины |
Инсулин | Галанин |
Холецистокинин-панкреозимин | Аминокислоты (глутамат и гамма-аминомасляная кислота) |
Глюкагоноподобный пептид | Кортизол |
Кокаин- и амфетамин-опосредованные транскрипты | Грелин |
Пептид YY | |
Гипоталамус и стволовые структуры мозга (такие как дугообразное ядро, паравентрикулярное ядро, ядро одиночного пути, дорзальное двигательное ядро блуждающего нерва и другие) участвуют в восприятии сигналов насыщения, опосредуемых гормонами, адипокинами, нейропептидами и их метаболитами и трансформации полученной информации в поведенческие реакции [6]. Преобразование периферического сигнала происходит при помощи нейротрансмиттеров, к которым относятся катехоламины (дофамин, адреналин и норадреналин) и индоламины (серотонин). К настоящему времени известно не менее пятидесяти химических соединений, которые способны функционировать в качестве синаптических медиаторов.
Дофамин, норадреналин и адреналин являются последовательными звеньями цепи превращений аминокислоты тирозина. Хотя дофаминергические нейроны составляют 1–2% от общей популяции нейронов, их роль в регуляции пищевого поведения крайне важна. Известно 5 типов рецепторов дофамина, которые разделены на 2 подтипа в зависимости от воздействия на аденилатциклазу – D1-подобные (D1, D5) – активирующие и D2-подобные (D2, D3, D4) – ингибируют ее. В настоящее время роль D1-подобных рецепторов в регуляции пищевого поведения не доказана. Роль D2-подобных рецепторов определяется не только их количеством, но и местом локализации [8, 9].
Норадреналин реализует свое действие в клетках паравентрикулярных и вентромедиальных ядер гипоталамуса. Воздействие на α1-, β2- и β3-адренорецепторы приводит к снижению аппетита, а стимуляция α2-рецепторов, наоборот, стимулирует аппетит.
Норадреналин и дофамин являются нейрогуморальными медиаторами на окончаниях постганглионарных нервных волокон и в некоторых отделах головного мозга. Самые высокие концентрации этих аминов встречаются в окончаниях нейронов, где они синтезируются и хранятся в везикулах в области расширенной концевой части. Из фенилаланина синтезируются три катехоламина: норадреналин, адреналин и дофамин. Ферменты, участвующие в биосинтезе норадреналина и адреналина, не обладают высокой специфичностью. Так, ДОФА-декарбоксилаза катализирует превращение 5-гидрокситриптофана в 5-ГТА и гистидина в гистамин. Адреналин, высвободившийся в синаптическую щель, разрушается частично, а часть его снова захватывается окончанием симпатического нейрона.
Одним из важнейших трансмиттеров, участвующих в регуляции энергетического гомеостаза, который заключается в стимуляции одних и ингибировании других нейронов гипоталамуса периферическими гормонами, является серотонин. Серотонин (5-гидрокситриптамин) 5-ГТА был выделен в 1948 г. Он представляет собой соединение, имеющее в организме человека функцию гормона и нейромедиатора. Серотонин обладает самыми разнообразными свойствами, обнаруживается в тканях, тучных клетках и тромбоцитах. Самая высокая его концентрация наблюдается в эпифизе и составляет от 60 до 180 мкг на грамм, где он служит предшественником для биосинтеза мелатонина. Серотонин синтезируется из триптофана, гидроксилирование которого приводит к образованию 5-гидрокситриптофана (5-ГТФ). Эта реакция катализируется 5-ГТФ-гидроксилазой. Декарбоксилирование 5-ГТФ ферментом 5-ГТФ-декарбоксилазой сопровождается образованием 5-гидрокситриптамина (серотонин, 5-НТ) [10]. Этот фермент декарбоксилирует также гистидин и ДОФА. В ЦНС и ЖКТ 5-ГТА депонируется в клеточных цитоплазматических гранулах, подобных хромаффинным гранулам, в которых депонируются катехоламины. Большинство серотонинергических нейронов находится в гипоталамусе и лимбической системе головного мозга. Больше всего их в так называемых «ядрах шва» – участках ствола мозга. Именно там и происходит синтез серотонина в головном мозге. Экзогенный серотонин не проникает через гематоэнцефалический барьер [11], таким образом, концентрация серотонина в головном мозге не зависит от синтеза и секреции его в ЖКТ, а определение концентрации серотонина в крови не дает информации о его концентрации в ЦНС. Однако для предшественника серотонина 5-ГТФ барьера проницаемости не существует.
Эффекты серотонина реализуются через его рецепторы. Выделено 14 типов серотониновых рецепторов: 5-НТ1A-F, 5-HT2A-C, 5HT3-7 [5]. Однако лишь для части рецепторов определена роль в патогенезе ожирения: 5-НТ2С, 5-НТ1А и 5-НТ2В [10, 12], а также все еще мало изученного 5-НТ6 [13]. Точкой приложения серотонина является меланокортиновая система. В дугообразных ядрах гипоталамуса серотонин активирует ПОМК/КАРТ-нейроны, что приводит к увеличению выработки α-МСГ и, соответственно, снижению потребления пищи, а взаимодействие с АПБ-нейронами предотвращает подавление секреции α-МСГ [5]. Серотонин, вырабатываемый в ЖКТ, также вносит вклад в энергетическую регуляцию, стимулируя моторику ЖКТ и секрецию соляной кислоты в желудке и бикарбонатов в двенадцатиперстной кишке, а также реализует вазоактивные свойства в слизистой и подслизистой оболочках и определяет вкусовые ощущения. Серотонин суживает кровеносные сосуды, в т.ч. почечные, менингеальные и легочные артерии. Он также суживает вены и венулы, но расширяет кровеносные сосуды скелетной мускулатуры, коронарные сосуды и капилляры кожи, провоцируя периферическое депонирование крови. На миокард 5-ГТА оказывает непосредственное слабое положительное инотропное и хронотропное действие, однако клинически у человека это практически не проявляется, поскольку серотонин также вызывает рефлекторную брадикардию. Серотонин влияет на артериальное давление, это влияние имеет вид трехфазного процесса: сначала наблюдается кратковременное понижение давления вследствие усиления активности блуждающего нерва, вызванного стимуляцией хеморецепторов коронарных сосудов и каротидного синуса, с последующим быстрым повышением АД вследствие сужения периферических сосудов. Позднее повышение АД сменяется стойкой гипотензией вследствие расширения кровеносных сосудов скелетной мускулатуры. Серотонин стимулирует все гладкомышечные структуры.
Серотонин содержится в нервной системе. Большие количества 5-ГТА обнаруживаются в области среднего мозга, лимбической системы, гипоталямуса, хвостатом ядре и гипофизе. 5-ГТА является химическим медиатором, высвобождающимся триптаминергическими нейронами, широко представленными в мозге. Одной из важных функций нейронов, где медиатором служит триптамин, является торможение повышенной реактивности на разные стимулы; изменение триптаминергических функций может быть причиной нарушения сна, настроения, восприятия боли, сексуального и пищевого поведения, моторной активности и восприятий [14]. Такие нейроны участвуют также в регуляции температуры тела, контроле за эндокринными функциями и экстрапирамидной активностью.
Нарушение метаболизма 5-ГТА в мозге является одной из предполагаемых причин определенных психических нарушений, в том числе нарушений пищевого поведения.
Для выработки серотонина в организме необходимо:
- поступление с пищей триптофана – аминокислоты, необходимой для непосредственного синтеза серотонина в синапсах [11];
- поступление глюкозы, стимуляция выброса инсулина в кровь, стимуляция катаболизма в тканях и, как следствие, – повышение уровня триптофана в крови.
С этими фактами напрямую может быть связана булимия и пристрастие к пище, богатой углеводами. Серотонин способен вызвать субъективное ощущение сытости, причем, когда в организм поступает пища, в том числе содержащая триптофан, увеличивается выработка серотонина, что повышает настроение. Мозг быстро улавливает связь между этими явлениями – и в случае депрессии (серотонинового голодания), незамедлительно «требует» дополнительного поступления пищи с триптофаном или глюкозой. Наиболее богаты триптофаном продукты, которые почти целиком состоят из углеводов, например, хлеб, бананы, шоколад или чистые углеводы: сахар или фруктоза.
Серотонин метаболизируется в организме с помощью моноаминоксидазы-А (МАО-А) до 5-гидроксииндолуксусной кислоты, которая затем выводится с мочой. Первые антидепрессанты являлись ингибиторами моноаминоксидазы, которые также подавляют разрушение норадреналина моноаминоксидазой. Однако из-за большого количества побочных эффектов, вызванных широким биологическим действием моноаминоксидазы, в настоящее время в качестве антидепрессантов применяются «ингибиторы обратного захвата серотонина». Эти вещества затрудняют и обратный захват серотонина в синапсах, тем самым повышая его концентрацию в крови. Отмечено, что помимо антидепрессивного действия они могут работать как аноректики [14]. В частности, ингибирование обратного захвата серотонина приводит к тому, что эффект серотонина, вызывающего деполяризацию ПОМК/КАРТ-нейронов, где сосредоточены рецепторы 5-НТ2С, повышение продукции α-MSH, активацию рецепторов МК4,3 реализуется в снижении количества принимаемой пищи.
Синапс – это структура, образованная тесным контактом нейрона с нейроном или с эффекторной клеткой. Он сформирован для передачи возбуждения или ингибирования. Синапс между преганглионарным и постганглионарным волокнами носит название ганглия, а между постганглионарным волокном и рецептором – нейроэффекторного соединения. Синапс является физиологическим, а не анатомическим продолжением нейрона. Переход импульса через синапс называется процессом передачи, тогда как движение импульса по волокну, преганглионарному или постганглионарному, – процессом проведения импульса. Пространство между пресинаптическими и постсинаптическими волокнами или между нервным окончанием и рецептором получило название синаптической щели. В области ганглия она ограничена пре- и постсинаптической мембраной, а в области нейроэффекторного соединения – поверхностной мембраной нервного окончания с одной стороны и зоной рецептора – с другой. Концевые части пре- и постганглионарных аксонов содержат овальные пузырьки – синаптические пузырьки, имеющие тенденцию к скоплению вблизи синаптической щели. При передаче нервного импульса нейромедиаторы из синаптических пузырьков попадают в синаптическую щель, после чего связываются с рецепторами на постсинаптической мембране. Затем они удаляются из синаптической щели, либо разрушаясь под действием ферментов, либо подвергаясь обратному захвату соответствующими рецепторами пресинаптической мембраны.
Действие лекарственных препаратов, связанное с медиаторами, можно классифицировать как пресинаптическое и постсинаптическое [15].
Многие лекарственные средства с центральным действием изменяют реакцию на 5-ГТА или процесс его депонирования, синтеза, захвата, высвобождения или катаболизма. Так как во многих исследованиях показана решающая роль серотонинергической недостаточности как причины нарушений пищевого поведения, применение ингибиторов обратного захвата серотонина актуально в лечении ожирения [16, 17]. Действительно, ожирение характеризуется более низким церебральным уровнем серотонина, это ведет к формированию отсроченного сигнала к прекращению еды (или его отсутствия), вследствие недостаточной рецепторной стимуляции. Снижение уровня серотонина компенсаторно увеличивает плотность рецепторов, приводит к развитию расстройств, напоминающих депрессивные.
Ингибиторы обратного захвата серотонина в синаптической щели конкурентно связываются с рецепторами обратного захвата 5-ГТА. В результате концентрация серотонина в синаптической щели увеличивается, что усиливает передачу нервного импульса. Этот эффект лежит в основе действия препаратов, повышающих психическую активность, снимающих эмоциональное напряжение и моделирующих пищевое поведение.
Сибутрамин
Сибутрамин представляет собой ингибитор обратного захвата нейромедиаторов: серотонина (53%), норадреналина (54%) и дофамина (16%) [18], вследствие чего возрастает концентрация этих медиаторов в синаптическом пространстве. Вследствие такого двойного механизма действия препарат оказывает влияние на обе стороны энергетического баланса, т.е., усиливая и пролонгируя чувство насыщения, уменьшает поступление энергии за счет снижения количества потребляемой пищи и увеличивает ее расход вследствие усиления термогенеза.
Сибутрамин образует в организме активные метаболиты (первичные и вторичные амины), значительно превосходящие сибутрамин по способности ингибировать обратный захват серотонина и норадреналина. Сибутрамин отличается по механизму действия от других препаратов центрального действия тем, что не влияет на допаминергическую систему и потому не вызывает привыкания и лекарственной зависимости.
Основные побочные эффекты препарата — сухость во рту, запоры, отсутствие аппетита, бессонница, повышение АД, учащение сердцебиения — слабо выражены и носят преходящий характер. Сибутрамин не назначают при беременности и лактации, при тяжелой почечной и печеночной недостаточности, психических заболеваниях, АГ, ИБС и нарушениях ритма сердца, сердечной недостаточности, феохромоцитоме, глаукоме, а также одновременно с ингибиторами моноаминооксидазы и психотропными препаратами. Начальную дозу сибутрамина (10 мг) применяют однократно утром. Если за 4 недели потеря массы тела составляет менее 2 кг, то при хорошей переносимости препарата доза может быть увеличена до 15 мг. Прием препарата прекращают, если за 3 месяца лечения масса тела уменьшилась менее чем на 5%. Длительность приема препарата не более 12 месяцев. Лечение сибутрамином помогает больным в формировании правильных привычек питания. В 1998 г. препарат был зарегистрирован в США, а через год и в Европе, как препарат для лечения ожирения.
По данным мета-анализа по оценке эффективности лечения ожирения, в который были включены 10 двойных слепых плацебо контролируемых исследований (n=2623) с длительностью приема препаратов от 1 года, пациенты, получавшие сибутрамин, снизили массу тела на 4,2 кг больше (95% ДИ от 3,6 до 4,7 кг), чем пациенты, получавшие плацебо, что увеличило число лиц, похудевших без медикаментозного лечения на 5% и 10% от исходного веса, на 32% и 18% соответственно [19]. Среди пациентов, получавших сибутрамин, было на 10–30% больше лиц, которые успешно удерживали достигнутый результат (успешным считали сохранение 80–100% потерянного веса). Аналогичные результаты были получены и по данным других мета-анализов [20]. Среди метаболических эффектов сибутрамина отмечено достоверное уменьшение ИМТ, окружности талии, снижение уровня ТГ, повышение уровня ЛПВП и небольшое снижение гликированного гемоглобина и тощаковой гликемии у пациентов с сахарным диабетом и ожирением. Применение сибутрамина приводило к повышению систолического и диастолического АД на 1–3 мм рт.ст. и увеличению частоты пульса на 4–5 ударов в минуту [18]. Наиболее распространенные побочные эффекты сибутрамина, такие как сухость во рту, анорексия, запор, головная боль и бессонница, как правило, связаны с симпатомиметическими свойствами, частота нежелательных явлений варьировала от 7 до 20%.
Исследование SCOUT (Sibutramine Cardiovascular OUTcomes) было запланировано ддя оценки исходов снижения массы на фоне фармакотерапии сибутрамином у пациентов с высоким сердечно-сосудистым риском. Из 10 742 пациентов, включенных в предварительный период исследования, абсолютное большинство (91,9 %) имели противопоказания к назначению препарата, предусмотренные действовавшей инструкцией: сердечно-сосудистые заболевания и артериальное давление выше 145/90 мм рт. ст. 6-недельный период лечения продемонстрировал хорошую переносимость и эффективность препарата у пациентов с высоким сердечно-сосудистым риском [29]. Далее SCOUT было продолжено как рандомизированное двойное слепое плацебо-контролируемое исследование, в которое было включено 9804 мужчин и женщин в возрасте ≥55 лет, с ИМТ≥27 кг/м2 и ≤45 кг/м2 или ≥25 кг/м2 и <27 кг/м2 при окружности талии ≥102/≥88 см (мужчины/женщины соответственно) [21]. Все пациенты имели в анамнезе сердечно-сосудистые заболевания, такие как ишемическая болезнь сердца, инсульт или облитерирующее поражение периферических сосудов и/или сахарный диабет 2-го типа с наличием хотя бы одного дополнительного кардиоваскулярного фактора риска (гипертензия, дислипидемия, курение или диабетическая нефропатия). Критериями исключения были симптомы сердечной недостаточности выше II функционального класса (классификация Нью-Йоркской кардиологической ассоциации), АД>160/100 мм рт. ст., пульс >100 ударов в минуту, планируемая операция на сердце или коронарных артериях, а также недавняя потеря веса. Средняя продолжительность лечения составила 3,4 года. По результатам исследования средняя потеря веса в течение вводного 6-недельного периода (сибутрамин в дозе 10 мг) составила 2,6 кг; после рандомизации пациенты, получавшие сибутрамин, продолжили дальнейшее снижение веса (-1,7 кг за год), тогда как пациенты группы плацебо отметили обратную прибавку веса (0,7 кг за год). В течение вводного периода отмечалось снижение артериального давления – в среднем на 4,7 мм рт.ст. систолического и 1,7 мм рт.ст. диастолического. После рандомизации средние показатели АД оставались ниже исходных значений в обеих группах наблюдения, но в группе сибутрамина они были статистически значимо выше, чем в группе плацебо – средние различия в группах составляли от -0,3 до 1,2 мм рт.ст. САД и от 0,6 до 1,4 мм рт.ст. ДАД. Частота пульса также была выше в группе сибутрамина – 3,7 и 2,2 удара в минуту соответственно. Было зафиксировано повышение риска первичных сердечно-сосудистых событий на 16% выше в группе сибутрамина, а число всех случаев составило 11,4% в группе сибутрамина по сравнению с 10,0% в группе плацебо; в том числе риск развития инфаркта миокарда без летального исхода и инсульта без летального исхода были 4,1% и 2,6% в группе сибутрамина и 3,2% и 1,9% в группе плацебо. При этом риск смерти от сердечно-сосудистых событий или смерти от всех причин был сравним с группой плацебо [21].
Дизайн исследования SCOUT вызвал целый ряд замечаний со стороны экспертов, а именно, включение в исследование пациентов, уже имеющих противопоказания к назначению сибутрамина, и большая продолжительность лечения (в среднем 3,4 года, тогда как инструкцией было предусмотрено непрерывное лечение только в течение 2 лет). Несмотря на это, в 2010 году по рекомендации американских и европейских органов по надзору за лекарственными препаратами (FDA, EMA) была полностью прекращена продажа препарата в странах Евросоюза, в США препарат был ограничен для применения у пациентов с сердечно-сосудистыми заболеваниями (ССЗ).
Отсутствие иных эффективных препаратов для лечения ожирения привело к дальнейшим исследованиям препарата, а также пересмотру исследования SCOUT – была продемонстрирована безопасность применения сибутрамина у пациентов с ССЗ в течение короткого периода лечения (до 6 мес) [22, 23], а также безопасность его краткосрочного [24, 25] и долгосрочного [26] применения у пациентов, не имеющих в анамнезе ССЗ.
В России опыт использования сибутрамина обобщен в виде результатов крупных наблюдательных программ. Так, в наблюдательной программе ВЕСНА (2011–2012) приняли участие более 34 тысяч пациентов и 1520 врачей в 52 городах Российской Федерации [25]. В рамках программы был проведен сбор эпидемиологических данных об эффективности и безопасности препарата Редуксин® (сибутрамин и микрокристаллическая целлюлоза) в условиях повседневной медицинской практики. Наблюдательная программа ВЕСНА во многом содействовала внедрению рациональной терапии лекарственными препаратами, содержащими сибутрамин, в России. Обоснованное назначение препарата врачами и систематическая оценка состояния пациента в процессе лечения способствовали профилактике целого ряда осложнений фармакотерапии ожирения и снижению частоты и выраженности возможных нежелательных явлений.
Программа «ПримаВера», проводимая под руководством Эндокринологического научного центра и Российской ассоциации эндокринологов, продолжила практику наблюдательных программ в сфере лечения таких социально значимых заболеваний, как ожирение и СД 2 типа, и была направлена на внедрение в клиническую практику врачей разных специальностей алгоритма мониторинга эффективности и безопасности терапии ожирения. Реализация этого алгоритма позволяет врачу любой специальности правильно отбирать пациентов, которым показано применение препарата Редуксин® (сибутрамин и микрокристаллическая целлюлоза), корректировать дозу в зависимости от результатов лечения и его влияния на сердечно-сосудистую систему, а также отслеживать на ранних сроках не ответивших на терапию пациентов, у которых дальнейшее применение сибутрамина может влиять на возрастание сердечно-сосудистых рисков. В программе приняли участие более 3000 врачей и около 100 000 пациентов. Результаты реализации программы «ПримаВера» подтвердили благоприятный профиль безопасности препарата Редуксин® в течение длительного периода лечения ожирения (до 1 года) и его высокую эффективность. Так, за 3 месяца терапии значимое снижение массы тела на 5% и более от исходных значений было отмечено у 92,4% больных. За двенадцать месяцев терапии у 51,2% пациентов ИМТ уменьшился до показателя ниже 30 кг/м2, а у 11,5% пациентов, имевших морбидное ожирение, удалось добиться снижения ИМТ ниже 40 кг /м2, 37,3% пациентов, завершивших терапию, достигли своей «идеальной» массы тела. При этом частота нежелательных явлений не превышала 2,5% случаев [26].
При длительном ограничении калорийности питания у пациентов часто наблюдается физиологическое наступление эффекта «плато», т.е. остановка в процессе снижения массы тела. В этот момент взаимодействие с врачом особенно важно для выяснения причин этой остановки, своевременной коррекции терапии, а также для преодоления снижения мотивации к продолжению лечения. Регулярное общение пациента с врачом, осуществляемое в рамках наблюдательных программ, позволяет это осуществить и добиться достижения желаемых результатов терапии. Среди пациентов, получавших длительную (более 3 мес.) терапию препаратом Редуксин® в дозе 10 мг, в 22,1% случаев (N=3 446) наблюдался эффект «плато». При этом важно отметить, что у пациентов, не ответивших на терапию Редуксином в течение трех месяцев, но продолживших лечение, эффект «плато» проявлялся в 1,7 раз чаще, чем у пациентов, соответствующих критерию «ответа» на терапию, однако носил временный характер. В целом, эффект «плато» носил временный характер у 20,4% (N=3 180) [27].
Еще одним параметром контроля терапии, который важно оценивать в рамках длительного (4–6 месяцев) применения Редуксина, является обратный набор массы тела, т.е. ее увеличение на 3 кг от ранее достигнутого. Среди пациентов, ответивших на терапию (по результатам 3 месяцев лечения), обратный набор массы тела зарегистрирован лишь в 0,41% случаев. Возможной причиной было отсутствие приверженности пациентов терапии и рекомендациям врача.
Таким образом, можно с уверенностью говорить о целесообразности как минимум шестимесячного курса терапии Редуксином для достижения целевого снижения массы тела на 10–14% от исходной и закрепления полученного результата, а также о возможности и целесообразности в зависимости от результатов лечения продления терапии до двенадцати месяцев.
Можно утверждать, что результаты снижения массы тела с помощью комбинированного препарата сибутрамина и микрокристаллической целлюлозы не только отвечают суррогатным критериям эффективности лечения (улучшение физиологических и биохимических показателей), но и способствуют достижению некоторых так называемых клинических конечных точек терапии – уменьшению частоты осложнений, связанных с заболеваниями, ассоциированными с ожирением, и улучшению качества жизни пациентов.
В последние годы появляются новейшие данные, иллюстрирующие безопасность применения сибутрамина в рамках инструкции. Так, большое когортное исследование (23 937 пациентов), посвященное оценке влияния назначения сибутрамина на кардиоваскулярные исходы в рутинной клинической практике, проведенное в Великобритании, результаты которого опубликованы в мае 2015 г., продемонстрировало низкий риск развития сердечно-сосудистых осложнений при приеме сибутрамина в группе пациентов без сердечно-сосудистых заболеваний [28]. Авторы пишут о том, что в рамках исследования SCOUT повышение риска возникновения нежелательных явлений наблюдалось у пациентов, которым противопоказано применение сибутрамина в соответствии с инструкцией по применению, соответственно, значимость результатов этого исследования для общей популяции больных ожирением весьма спорна. В заключение, был сделан вывод о том, что разрешение на использование сибутрамина для группы пациентов без сердечно-сосудистых заболеваний было отозвано необоснованно.
Таким образом, ожирение зачастую связано с изменением функциональной организации гипоталамуса или прочих нервных центров, отвечающих за пищевое поведение, а также с нарушением метаболизма некоторых нейромедиаторов, что определяет обоснованность назначения препаратов центрального действия подобным пациентам. Сибутрамин в комбинации с микрокристаллической целлюлозой (Редуксин®), назначаемый в соответствии с инструкцией по медицинскому применению, позволяет обеспечить безопасное и эффективное лечение ожирения и способствует уменьшению частоты осложнений коморбидных состояний и улучшению качества жизни пациентов.
Информация о финансировании и конфликте интересов
Авторы заявляют об отсутствии явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Работа выполнена без привлечения дополнительного финансирования со стороны третьих лиц.
1. Диагностика и лечение ожирения у взрослых. Рекомендации Российской ассоциации эндокринологов. Под редакцией И.И. Дедова. – Москва, 2010. [Diagnostika I lechenie ozhireniya u vzroslyh. Rekomendacii Rossijskoj Associacii Ehndokrinologov. Ed by Dedov I.I. Moscow; 2010 (In Russ.)]
2. Carnell S, Gibson C, Benson L, et al. Neuroimaging and obesity: current knowledge and future directions. Obes Rev. 2012;13(1):43-56. doi: 10.1111/j.1467-789X.2011.00927.x.
3. Кремнева Е.И., Суслин А.С., Говорин А.H., и др. фМРТ-картирование алиментарных зон головного мозга. Анналы клинической и экспериментальной неврологии. Том 9. №1 2015; 32-36. [Kremneva EI, Suslin AS, Govorin AN, et al. Mapping of the brain regions responsible for eating behavior regulation with functional MRI. Annals of clinical and experimental neurology. 2015;9(1): 32-36 (In Russ.)]
4. Ожирение. Под редакцией Дедова И.И., Мельниченко Г.А. / Москва: Медицинское информационное агентство, 2004. [Obesity. Ed by Dedov II, Melnichenko GA. Moscow: Medicinskoe informacionnoe agenstvo; 2004 (In Russ.)]
5. Yeo G, Heisler L. Unraveling the brain regulation of appetite: lessons from genetics. Nat Neurosci 2012; 15 (10): 1343–1349. doi: 10.1038/nn.3211.
6. Fry M, Hoyda T, Ferguson A. Making sense of it: roles of the sensory circumventricular organs in feeding and regulation of energy homeostasis. Exp Biol Med (Maywood) 2007; 232: 14–26.
7. Гайтон А.К., Холл Д.Э. Медицинская физиология. Москва: Логосфера, 2008.- 1296с. [Gayton AK, Kholl DE. Textbook of Medical Physiology. Moscow: Logosfera, 2008; 1296 (In Russ.)].
8. Guo J, Simmons W, Herscovitch P, et al. Striatal dopamine D2-like receptor correlation patterns with human obesity and opportunistic eating behavior. Mol Psychiatry. 2014;19 (10): 1078-84. doi: 10.1038/mp.2014.102
9. Van Strien T, Snoek H, Van der Zwaluw C, Engels R. Parental control and the dopamine D2 receptor gene (DRD2) interaction on emotional eating in adolescence. Appetite. 2010; 54 (2): 255-61. doi: 10.1016/j.appet.2009.11.006
10. Lam D, Garfield A, Marston O, et al. Brain serotonin system in the coordination of food intake and body weight. Pharmacol Biochem Behav 2010; 97 (1): 84–91. doi:10.1016/j.pbb.2010.09.003.
11. Best J, Nijhout H, Reed M. Serotonin synthesis, release and reuptake in terminals: a mathematical model. Theoretical Biology and Medical Modelling 2010; 7: 34. doi:10.1186/1742-4682-7-34
12. Heath MJ, Hen R. Serotonin receptors. Genetic insights into serotonin function. Curr Biol. 1995; 5: 997–999. doi: 10.1016/S0960-9822(95)00199-0
13. Garfielda A, Burkea L, Shawa J, et al. Distribution of cells responsive to 5-HT6 receptor antagonist-induced hypophagia. Behavioural Brain Research 2014; 266: 201–206. doi: 10.1016/j.bbr.2014.02.018
14. Wurtman R, Wurtman J. Brain serotonin, carbohydrate-craving, obesity and depression.
15. Obes Res. 1995; 3 (4): 477-480 doi: 10.1002/j.1550-8528.1995.tb00215.x
16. Satoskar RS, Bhandarkar SD, Rege NN. Pharmacology and Pharmacotherapeutics; 20th ed. Mumbai: Popular Prakashan; 2007.
17. Smith S, Weissman N, Anderson C, et al. Multicenter, placebo-controlled trial of lorcaserin for weight management. N Engl J Med. 2010; 363 (3): 245–256. doi: 10.1056/NEJMoa0909809
18. Chan E, He Y, Chui C, et al. Efficacy and safety of lorcaserin in obese adults: a meta-analysis of 1-year randomized controlled trials (RCTs) and narrative review on short-term RCTs. Obes Rev. 2013;14 (5): 383-92. doi: 10.1111/obr.12015.
19. Karam J, McFarlane S. Tackling obesity: new therapeutic agents for assisted weight loss. Diabetes Metab Syndr Obes. 2010; 3: 95–112
20. Rucker D, Padwal R, Li S, et al. Long term pharmacotherapy for obesity and overweight: updated meta-analysis. BMJ. 2007; 335 (7631): 1194–1199. doi:10.1136/bmj.39385.413113.25
21. Zhou YH, Ma XQ, Wu C, et al. Effect of anti-obesity drug on cardiovascular risk factors: a systematic review and meta-analysis of randomized controlled trials. PLoS One. 2012; 7(6): e39062. doi: 10.1371/journal.pone.0039062
22. James W, Caterson I, Coutinho W, et al. SCOUT Investigators Effect of sibutramine on cardiovascular outcomes in overweight and obese subjects. N Engl J Med. 2010; 363 (10): 905–917. doi: 10.1056/NEJMoa1003114
23. Seimon R., Espinoza D., Ivers L. et al. Changes in body weight and blood pressure: paradoxical outcome events in overweight and obese subjects with cardiovascular disease. Int J Obes. 2014;38(9): 1165-1171 doi: 10.1038/ijo.2014.2.
24. Caterson I, Finer N, Coutinho W, et al. Maintained intentional weight loss reduces cardiovascular outcomes: results from the Sibutramine Cardiovascular OUTcomes (SCOUT) trial. Diabetes, Obesity and Metabolism. 2012; 14 (6): 523-30. doi: 10.1111/j.1463-1326.2011.01554.x.
25. Pavlik V, Fajfrova J, Slovacek L, Drahokoupilova E. The role of sibutramine in weight reduction. Bratisl Lek Listy. 2013; 114 (3): 155-157.
26. Аметов А.С. Отчет о программе ВЕСНА. Эффективное лечение ожирения – путь борьбы с эпидемией Diabetus mellipidus. // Эффективная фармакотерапия. Спецвыпуск. — 2013. — С. 7-11. [Ametov AS. Otchet o programme VESNA. Effektivnoe lechenie ozhireniya – put borbyi s epidemiey Diabetus mellipidus. Effektivnaya farmakoterapiya. Special edition. 2013; 7-11. (In Russ.)].
27. Мельниченко Г.А., Романцова Т.И., Журавлева М.В.. Всероссийская программа безопасного снижения веса «ПримаВера». Итоги первого года проведения. Ожирение и метаболизм. 2014; 1(38): 62-67. [Melnichenko GA, Romantsova TI, Zhuravleva MV. Vserossiyskaya programma bezopasnogo snizheniya vesa «PrimaVera». Itogi pervogo goda provedeniya. Obesity and metabolism. 2014; 1(38): 62-67. (In Russ.)]. doi:10.14341/omet2014162-68
28. Трошина Е.А., Мазурина Н.В., Галиева М.О. Создание стратегий лечения ожирения и коморбидных заболеваний на основе наблюдательных программ: промежуточные результаты всероссийской наблюдательной программы ПримаВера. // Альманах клинической медицины. – 2015. – №S1. – С. 95-101. [Troshina EA, Mazurina NV, Galieva MO. Development of therapeutic strategies for obesity and comorbid disorders based on observational programs: interim results of the Russian observational program PrimaVera. Almanah klinicheskoj mediciny. 2015; (S1): 95-101 (In Russ.)].
29. Hayes JF, Bhaskaran K, Batterham R, Smeeth L, Douglas I. The effect of sibutramine prescribing in routine clinical practice on cardiovascular outcomes: a cohort study in the United Kingdom. Int J Obes.. 2015;39(9):1359-1364. doi:10.1038/ijo.2015.86.
30. Caterson I, Coutino V, Finer N et al. Early response to sibutramine in patients not meeting current label criteria: preliminary analysis of SCOUT lead-in period. Obesity (Silver Spring). 2010;18(5):987-94. doi: 10.1038/oby.2009.327.
РЕЗЕРВЫ МИКРОЦИРКУЛЯЦИИ И РЕАКТИВНОСТЬ ТКАНЕВОГО МЕТАБОЛИЗМА У БОЛЬНЫХ ИБС ПРИ РАЗЛИЧНОЙ СТАДИИ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ | Клинкова
1. Mareev VYu, Ageev FT, Arutyunov GP, et al. SEHF, RSC and RSMSIM national guidelines on CHF diagnostics and treatment (fourth revision). Zhurnal Serdechnaya Nedostatochnost’ 2013; 14(7): 379-472. Russian (Мареев В. Ю., Агеев Ф. Т., Арутюнов Г. П. и др. Национальные рекомендации ОССН, РКО и РНМОТ по диагностике и лечению ХСН (четвертый пересмотр). Журнал Сердечная Недостаточность 2013, 14(7): 379-472).
2. Menghini R, Casagrande V, Federici M. MicroRNAs in endothelial senescence and atherosclerosis. J Cardiovasc Transl Res 2013; 6(6): 924-30.
3. Levicheva EN, Kamenskaya OV, Loginova IYu. Reserve opportunities of microcirculatory blood flow in peripheral tissues circulatory hypoxia. Regionarnoe krovoobrashchenie i mikrotsirkulyatsiya. 2012; 11(3): 34-8. Russian (Левичева Е.Н., Каменская О.В., Логинова И.Ю. Резервные возможности микроциркуляторного кровотока периферических тканей при циркуляторной гипоксии. Регионарное кровообращение и микроциркуляция 2012, 11(3): 34-8).
4. Belenkov IuN, Privalova EV, Danilogorskaia IuA, et al. Structural and functional changes in capillary microcirculation in patients with cardiovascular diseases (arterial hypertension, coronary heart disease, chronic heart failure) observed during computer videocapillaroscopy. Kardiologiya i serdechno-sosudistaya khirurgiya 2012; 5(2): 49-56. Russian (Беленков Ю.Н., Привалова Е.В., Данилогорская Ю.А. и др. Структурные и функциональные изменения микроциркуляторного русла на уровне капилляров, у больных сердечно-сосудистыми заболеваниями (артериальная гипертония, ишемическая болезнь сердца, хроническая сердечная недостаточность), которые можно наблюдать в ходе компьютерной видеокапилляроскопии. Кардиология и сердечно-сосудистая хирургия. 2012, 5(2): 49-56).
5. Barhatov IV. Laser Doppler flowmetry for human blood microcirculation assessment Kazanskij meditsinskij zhurnal 2014; 95(1): 63-9. Russian (Бархатов И.В. Применение лазерной допплеровской флоуметрии для оценки нарушений системы микроциркуляции крови человека. Казанский медицинский журнал 2014, 95(1): 63-9).
6. Kozlov VI, Azizov GA, Gurova OA, et al. Laser Doppler flowmetry in the assessment of microcirculatory disorders and blood M.: Izd-vo RUDN; 2012. Russian (Козлов В. И., Азизов Г.А., Гурова О.А. и др. Лазерная допплеровская флоуметрия в оценке состояния и расстройств микроциркуляции крови. М.: Изд-во РУДН; 2012).
7. Dedov II, Shestakova MV, Maksimova MA. Diabetes Mellitus. Federal Program. M.: MediaSphera; 2002. Russian (Дедов И. И., Шестакова М.В., Максимова М. А. Федеральная целевая программа “Сахарный диабет”. М.: Медиа Сфера; 2002).
8. Kamenskaya OV, Klinkova AS, Karpenko AA, et al. Peripheral microcircuiation in patients over 60 years with atherosclerosis of lower limb arteries. Patologiya krovoobrashheniya i kardiokhirurgiya 2013; 3: 22-6. Russian (Каменская О.В., Клинкова А.С., Карпенко А.А. и др. Периферическая микроциркуляция у пациентов старше 60 лет с хронической ишемией нижних конечностей. Патология кровообращения и кардиохирургия 2013, 3: 22-6).
9. Kamenskaya OV, Klinkova AS, Karpenko AA, et al. The functional state of peripheral perfusion in patients with combined lower limb ischemia and Type 2 diabetes mellitus during revascularization of the main arteries. Patologiya krovoobrashheniya i kardiokhirurgiya 2015; 19(1): 78-83. Russian (Каменская О.В., Клинкова А.С., Карпенко А.А. и др. Функциональное состояние периферической перфузии у больных ишемией нижних конечностей в сочетании с сахарным диабетом 2 типа при реваскуляризации магистральных артерий. Патология кровообращения и кардиохирургия. 2015, 19(1): 78-83).
10. Gurfinkel YuI, Kudutkina MI, Parfenova LM, et al. Microcirculation in chronic heart failure patients treated with ACE inhibitors and diuretics. Russ J Cardiol 2011; 2: 43-8. Russian (Гурфинкель Ю. И., Кудуткина М. И., Парфенова Л.М. и др. Особенности микроциркуляции у больных хронической сердечной недостаточностью на фоне лечения ингибиторами АПФ и диуретиками. Российский кардиологический журнал 2011, 2: 43-8).
11. Muiesan ML, Salvetti M, Rizzoni D, et al. Pulsatile Hemodynamics and Microcirculation Evidence for a Close Relationship in Hypertensive Patients. Hypertension 2013; 61(1): 130-6.
12. Mohammed SF, Hussain S, Mirzoyev SA, et al. Coronary microvascular rarefaction and myocardial fibrosis in heart failure with preserved ejection fraction. Circulation 2015; 131(6): 550-9.
13. Moore KJ, Tabas I. Macrophages in the pathogenesis of atherosclerosis. Cell 2011; 145(3): 341-55.
14. Ed Rainger G, Chimen M, Harrison MJ, et al. The role of platelets in the recruitment of leukocytes during vascular disease. Platelets. 2015; 26(6): 507-20.
15. Konopleva LF. Endothelial dysfunction in the pathogenesis of cardiovascular disease and methods of its correction Therapia 2011; 3(56): 26-30. Russian (Коноплева Л.Ф. Эндотелиальная дисфункция в патогенезе сердечно-сосудистых заболеваний и методы ее коррекции Терапия 2011, 3(56): 26-30).
16. Hellmann M, Roustit M, Cracowski JL. Skin microvascular endothelial function as a biomarker in cardiovascular diseases? Pharmacol Rep. 2015; 67(4): 803-10.
17. Makolkin VI, Podzolkov VI, Bran’ko VV, et al. Microcirculation in cardiology M.: Vizart; 2004. Russian (Маколкин В. И., Подзолков В. И., Бранько В.В. и др. Микроциркуляция в кардиологии. М.: Визарт; 2004).
18. Xu Y, Arora RC, Hiebert BM, et al. Non-invasive endothelial function testing and the risk of adverse outcomes: a systematic review and meta-analysis. Eur Heart J Cardiovasc Imaging. 2014; 15(7): 736-46.
19. Lazarenko VA, Bobrovskaya EA, Sorokin AV. Hyperhomocysteinemia: peripheral atherosclerosis and reconstructive surgery Kurskij nauchno-prakticheskij vestnik “Chelovek i ego zdorov’e” 2014; 4: 63-6. Лазаренко В.А., Бобровская Е.А., Сорокин А.В. Гипергомоцистеинемия: периферический атеросклероз и реконструктивная хирургия. Курский научно-практический вестник «Человек и его здоровье”. 2014, 4: 63-6.
20. McCully KS Homocysteine and the pathogenesis of atherosclerosis. Expert Rev Clin Pharmacol. 2015; 8(2): 211-9.
И МЕТАБОЛИЗМА НЕЙТРОФИЛОВ КРОВИ У БОЛЬНЫХ РАСПРОСТРАНЕННЫМ ГНОЙНЫМ ПЕРИТОНИТОМ В ДИНАМИКЕ ПОСЛЕОПЕРАЦИОННОГО ПЕРИОДА | Савченко
1. Кнорре Д.Г., Мызина С.Д. Биологическая химия. Новосибирск: Изд-во СО РАН. 2012. 456 с. [Knorre D.G., Myzina S.D. Biologicheskaya khimiya [Biological chemistry]. Novosibirsk: Publishing House of the Siberian Branch of the Russian Academy of Sciences, 2012. 456 p.]
2. Кудрявцев И.В., Субботовская А.И. Опыт измерения параметров иммунного статуса с использованием шестицветного цитофлуоримерического анализа // Медицинская иммунология. 2015. Т. 17, № 1. С. 19–26. [Kudryavtsev I.V., Subbotovskaya A.I. Application of six-color f low cytometric analysis for immune profile monitoring. Meditsinskaya immunologiya = Medical Immunology (Russia), 2015, vol. 17, no. 1, pp. 19–26. doi: 10.15789/1563-0625-2015-1-19-26 (In Russ).]
3. Савченко А.А. Определение активности NAD(P)-зависимых дегидрогеназ в нейтрофильных гранулоцитах биолюминесцентным методом // Бюллетень экспериментальной биологии и медицины. 2015. Т. 159, № 5. С. 656–660. [Savchenko A.A. Evaluation of NAD(P)-dependent dehydrogenase activities in neutrophilic granulocytes by the bioluminescent method. Byulleten’ eksperimental’noi biologii i meditsiny = Bulletin of Experimental Biology and Medicine, vol. 159, no. 5, pp. 656–660. doi: 10.1007/s10517-015-3049-8 (In Russ).]
4. Савченко А.А., Здзитовецкий Д.Э., Борисов А.Г. Иммунометаболические нарушения при распространенном гнойном перитоните. Новосибирск: Наука, 2013. 142 с. [Savchenko A.A., Zdzitoveckij D.Je., Borisov A.G. Immunometabolicheskie narusheniya pri rasprostranennom gnoinom peritonite [Immune and metabolic disorders by the widespread purulent peritonitis]. Novosibirsk: Nauka, 2013. 142 p.]
5. Ярилин А.А. Иммунология. М.: ГЭОТАР-Медиа, 2010. 752 с. [Yarilin A.A. Immunologiya [Immunology]. Moscow: GEOTAR-Media, 2010, 752 p.]
6. Akram M. Citric acid cycle and role of its intermediates in metabolism. Cell Biochem. Biophys., 2014, vol. 68, no. 3, pp. 475–478. doi: 10.1007/s12013-013-9750-1
7. Azevedo E.P., Rochael N.C., Guimarães-Costa A.B., De Souza-Vieira T.S., Ganilho J., Saraiva E.M., Palhano F.L., Foguel D. A metabolic shift toward pentose phosphate pathway is necessary for amyloid fibriland phorbol 12-myristate 13-acetate-induced neutrophil extracellular trap (NET) formation. J. Biol. Chem., 2015, vol. 290, no. 36, pp. 22174–22183. doi: 10.1074/jbc.M115.640094
8. Boer K., Vogelsang H., Deufel T., Pfister W., Kiehntopf M. CD62L on neutrophil granulocytes, a useful, complementary marker for the prediction of ventriculitis in blood-containing CSF. Clin. Biochem., 2010, vol. 43, no. 16–17, pp. 1351–1355. doi:10.1016/j.clinbiochem.2010.07.003
9. Couto N., Wood J., Barber J. The role of glutathione reductase and related enzymes on cellular redox homoeostasis network. Free Radic. Biol. Med., 2016, vol. 95, pp. 27–42. doi: 10.1016/j.freeradbiomed.2016.02.028
10. Dang Y., Lou J., Yan Y., Yu Y., Chen M, Sun G, Li N. The role of the neutrophil Fcγ receptor I (CD64) index in diagnosing spontaneous bacterial peritonitis in cirrhotic patients. Int. J. Infect. Dis., 2016. vol. 49, pp. 154–160. doi: 10.1016/j.ijid.2016.06.021
11. De Jong E., De Lange D.W., Beishuizen A., Van de Ven P.M., Girbes A.R., Huisman A. Neutrophil CD64 expression as a longitudinal biomarker for severe disease and acute infection in critically ill patients. Int. J. Lab. Hematol., 2016, vol. 38, no. 5, pp. 576–584. doi: 10.1111/ijlh.12545
12. Deng X., Deng T., Ni Y., Zhan Y., Huang W., Liu J., Liao C. Cytochrome c modulates the mitochondrial signaling pathway and polymorphonuclear neutrophil apoptosis in bile duct-ligated rats. Exp. Ther. Med., 2016, vol. 12, no. 1, pp. 333–342. doi: 10.3892/etm.2016.3313
13. Genel F., Atlihan F., Gulez N., Kazanci E., Vergin C., Terek D.T., Yurdun O.C. Evaluation of adhesion molecules CD64, CD11b and CD62L in neutrophils and monocytes of peripheral blood for early diagnosis of neonatal infection. World J. Pediatr., 2012, vol. 8, no. 1, pp. 72–75. doi: 10.1007/s12519011-0304-6
14. Lavoie-Lamoureux A., Moran K., Beauchamp G., Mauel S., Steinbach F., Lefebvre-Lavoie J., Martin J.G., Lavoie J.P. IL-4 activates equine neutrophils and induces a mixed inf lammatory cytokine expression profile with enhanced neutrophil chemotactic mediator release ex vivo. Am. J. Physiol. Lung Cell Mol. Physiol., 2010, vol. 299, no. 4, pp. L472–L482. doi: 10.1152/ajplung.00135.2009
15. Macedo L.W., Cararo J.H., Maravai S.G., Gonçalves C.L., Oliveira G.M., Kist L.W., Guerra Martinez C., Kurtenbach E., Bogo M.R., Hipkiss A.R., Streck E.L., Schuck P.F., Ferreira G.C. Acute carnosine administration increases respiratory chain complexes and citric acid cycle enzyme activities in cerebral cortex of young rats. Mol. Neurobiol., 2016, vol. 53, no. 8, pp. 5582–5590. doi: 10.1007/s12035-015-9475-9
16. Maecker H., McCoy P., Nussenblatt R. Standardizing immunophenotyping for the human immunology project. Nat. Rev. Immunol., 2012, vol. 12, pp. 191–200. doi: 10.1038/nri3158
17. Mastej K., Adamiec R. Neutrophil surface expression of CD11b and CD62L in diabetic microangiopathy. Acta Diabetol., 2008, vol. 45, no. 3, pp. 183–190. doi:10.1007/s00592-008 -0040-0
18. Peters B.M., Noverr M.C. Candida albicans-Staphylococcus aureus polymicrobial peritonitis modulates host innate immunity. Infect. Immun., 2013, vol. 81, no. 6, pp. 2178–2189. doi: 10.1128/IAI.00265-13
19. Pliyev B.K., Sumarokov A.B., Buriachkovskaia L.I., Menshikov M. Extracellular acidosis promotes neutrophil transdifferentiation to MHC class II-expressing cells. Cell Immunol., 2011, vol. 271, no. 2, pp. 214–218. doi: 10.1016/j.cellimm.2011.08.020
20. Qian W., Huang G.Z. Neutrophil CD64 as a marker of bacterial infection in acute exacerbations of chronic obstructive pulmonary disease. Immunol. Invest., 2016, vol. 45, no. 6, pp. 490 –503. doi: 10.1080/08820139.2016.1177540.
21. Rodríguez-Espinosa O., Rojas-Espinosa O., Moreno-Altamirano M.M., López-Villegas E.O., Sánchez-García F.J. Metabolic requirements for neutrophil extracellular traps formation. Immunology, 2015, vol. 145, no. 2, pp. 213–224. doi: 10.1111/imm.12437
22. Sato T., Yoshida Y., Morita A., Mori N., Miura S. Glycerol-3-phosphate dehydrogenase 1 deficiency induces compensatory amino acid metabolism during fasting in mice. Metabolism, 2016, vol. 65, no. 11, pp. 1646–1656. doi: 10.1016/j.metabol.2016.08.005
23. Schuster D.P., Brody S.L., Zhou Z., Bernstein M., Arch R., Link D., Mueckler M. Regulation of lipopolysaccharide-induced increases in neutrophil glucose uptake. Am. J. Physiol. Lung Cell Mol. Physiol., 2007, vol. 292, no. 4, pp. L845–L851. doi: 10.1152/ajplung.00350.2006
24. Shashidharan P., Plaitakis A. The discovery of human of GLUD2 glutamate dehydrogenase and its implications for cell function in health and disease. Neurochem. Res., 2014, vol. 39, no. 3, pp. 460 –470. doi: 10.1007/s11064-013-1227-5
25. Sutton B.J., Davies A.M. Structure and dynamics of IgE-receptor interactions: FcεRI and CD23/FcεRII. Immunol. Rev., 2015, vol. 268, no. 1, pp. 222–235. doi:10.1111/imr.12340
26. Van der Meer W., Stephen Scott C., Verlaat C., Gunnewiek J.K., Warris A. Measurement of neutrophil membrane CD64 and HLA-DR in a patient with abdominal sepsis. J. Infect., 2006, vol. 53, no. 1, pp. e43–e46. doi: 10.1016/j.jinf.2005.09.003
27. Ventura I., Vega A., Chacón P., Chamorro C., Aroca R., Gómez E., Bellido V., Puente Y., Blanca M., Monteseirín J. Neutrophils from allergic asthmatic patients produce and release metalloproteinase-9 upon direct exposure to allergens. Allergy, 2014, vol. 69, no. 7, pp. 898–905. doi: 10.1111/all.12414
28. Verschoor C.P., Loukov D., Naidoo A., Puchta A., Johnstone J., Millar J., Lelic A., Novakowski K.E., Dorrington M.G., Loeb M., Bramson J.L., Bowdish D.M. Circulating TNF and mitochondrial DNA are major determinants of neutrophil phenotype in the advanced-age, frail elderly. Mol. Immunol., 2015, vol. 65, no. 1, pp. 148–156. doi: 10.1016/j.molimm.2015.01.015
29. Walmsley S.R., Whyte M.K. Neutrophil energetics and oxygen sensing. Blood, vol. 123, no. 18, pp. 2753–2754. doi: 10.1182/blood-2014-03-560409
Главврач назвал основным диагнозом Навального нарушение обмена веществ
Основной диагноз госпитализированного оппозиционера Алексея Навального — нарушение обмена веществ, заявил главный врач омской больницы скорой помощи №1 Александр Мураховский.
«На сегодняшний день у нас есть рабочие диагнозы. Основной из них, к которому мы склоняемся,— нарушение углеводного баланса, то есть, нарушение обмена веществ»,— сказал господин Мураховский. Он допустил, что это может быть вызвано резким понижением уровня сахара в крови.
Нарушение обмена веществ, резкое падение уровня сахара в крови. Заявление Александра Мураховского, главврача больницы, где лежит Алексей Навальный. pic.twitter.com/MxQEoXbvJE
— The Insider (@the_ins_ru) August 21, 2020
Врачи омской больницы впервые огласили диагноз господина Навального, до этого они ссылались на закон о защите персональных данных. Заместитель главного врача омской больницы Анатолий Калиниченко ранее утверждал, что диагноз устно сообщили жене и брату господина Навального. Юлии и Олегу Навальным не сообщали диагноз, а то, что им рассказали — это «набор симптомов, который может быть интерпретирован по-разному», заявила пресс-секретарь политика Кира Ярмыш.
Оксибутираты и барбитураты в крови господина Навального не найдены, сказал главврач. Ранее его заместитель Анатолий Калиниченко говорил, что в крови и моче политика яды или их следы не обнаружены. Вещество, найденное на коже и одежде господина Навального — это материал пластикового стаканчика, «обычная промышленная химия», отметил Мураховский. В крови пациента, по его словам, этого компонента нет.
Ранее сегодня директор Фонда борьбы с коррупцией (ФБК) Иван Жданов заявлял, что транспортная полиция сообщила им о смертельно опасном веществе. Транспортная полиция была в больнице, чтобы помочь с транспортировкой Навального медицинским бортом в Германию. Однако к моменту, когда самолет приземлился в аэропорту Омска, врачи заявили о нетранспортабельности господина Навального. По словам господина Калиниченко, из-за перепадов давления во время полета состояние пациента может ухудшиться.
Пресс-секретарь президента Дмитрий Песков заявил, что для транспортировки Алексея Навального нужно только решение лечащего врача. Накануне господин Песков заявлял, что Кремль готов содействовать переводу господина Навального для лечения за рубеж. В ответ лидер «Альянса врачей» Анастасия Васильева сообщила, что откликнулась на предложение. Спустя день господин Песков сказал, что не получал обращения как такового, но «лишняя бюрократия» в этом случае не нужна.
Напомним, 20 августа господин Навальный был госпитализирован в омскую больницу и впал в кому. Ему стало плохо во время перелета из Томска в Москву. Соратники оппозиционера уверены, что господина Навального отравили веществом, подсыпанным в чай, и настаивают на проведении анализов и лечении за границей. Состояние господина Навального улучшилось к утру 21 августа, при этом в течение дня оно остается нестабильным — это, по заявлению омских врачей, не позволяет перевезти его в другую клинику.
Что такое метаболизм?
Метаболизм — это термин, который используется для описания всех химических реакций, участвующих в поддержании живого состояния клеток и организма. Обмен веществ можно условно разделить на две категории:
- Катаболизм — распад молекул для получения энергии
- Анаболизм — синтез всех соединений, необходимых клеткам
Метаболизм тесно связан с питанием и доступностью питательных веществ.Биоэнергетика — это термин, который описывает биохимические или метаболические пути, с помощью которых клетка в конечном итоге получает энергию. Формирование энергии — один из жизненно важных компонентов обмена веществ.
Изображение предоставлено: VectorMine / Shutterstock.com
Питание, обмен веществ и энергия
Питание — это ключ к обмену веществ. Пути метаболизма зависят от питательных веществ, которые они расщепляют, чтобы произвести энергию. Эта энергия, в свою очередь, требуется организму для синтеза таких молекул, как новые белки и нуклеиновые кислоты (ДНК, РНК).
Питательные вещества, связанные с метаболизмом, включают такие факторы, как потребности организма в различных веществах, индивидуальные функции организма, необходимое количество и уровень, ниже которого ухудшается состояние здоровья.
Основные питательные вещества обеспечивают энергию (калории) и поставляют необходимые химические вещества, которые сам организм не может синтезировать. Пища содержит множество веществ, которые необходимы для построения, содержания и восстановления тканей тела, а также для его эффективного функционирования.
Диета нуждается в основных питательных веществах, таких как углерод, водород, кислород, азот, фосфор, сера и около 20 других неорганических элементов. Основные элементы представлены углеводами, липидами и белком. Кроме того, необходимы витамины, минералы и вода.
Углеводы в обмене веществ
Продукты питания содержат углеводы в трех формах: крахмал, сахар и целлюлозу (клетчатку). Крахмал и сахар являются основными и необходимыми источниками энергии для человека. Волокна увеличивают объем рациона.
Ткани организма зависят от глюкозы во всех сферах деятельности. Углеводы и сахара производят глюкозу в результате пищеварения или метаболизма.
Общая реакция горения глюкозы записывается как:
C 6 H 12 O 6 + 6 O 2 ——> 6 CO 2 + 6 H 2 O + энергия
Большинство людей потребляют около половины своего рациона в виде углеводов. Это происходит из таких продуктов, как рис, пшеница, хлеб, картофель и макаронные изделия.
Белки в обмене веществ
Белки являются основными строителями тканей в организме. Они являются частью каждой клетки тела. Белки помогают в структуре клеток, функциях, образовании гемоглобина для переноса кислорода, ферментах для выполнения жизненно важных реакций и множестве других функций в организме. Белки также жизненно важны для снабжения азотом генетического материала ДНК и РНК и производства энергии.
Белки необходимы для питания, поскольку содержат аминокислоты. Из 20 или более аминокислот человеческий организм не может синтезировать 8, и они называются незаменимыми аминокислотами.
К незаменимым аминокислотам относятся:
- Лизин
- Триптофан
- метионин
- лейцин
- Изолейцин
- Фенилаланин
- Валин
- Треонин
Продукты с высоким содержанием белка — яйца, молоко, соевые бобы, мясо, овощи и зерновые.
Жир в обмене веществ
Жиры — это концентрированные источники энергии. Они производят в два раза больше энергии, чем углеводы или белки, в пересчете на вес.
Функции жиров включают:
- Помогает формировать клеточную структуру;
- Образует защитную подушку и изоляцию вокруг жизненно важных органов;
- Способствует усвоению жирорастворимых витаминов,
- Обеспечение резервного хранилища энергии
Незаменимые жирные кислоты включают ненасыщенные жирные кислоты, такие как линолевая, линоленовая и арахидоновая кислоты. Их нужно принимать с пищей. Насыщенные жиры, наряду с холестерином, участвуют в артериосклерозе и сердечных заболеваниях.
Минералы и витамины в обмене веществ
Минералы, содержащиеся в пищевых продуктах, не вносят прямого вклада в энергетические потребности, но важны как регуляторы организма и играют роль в метаболических путях организма. В организме человека содержится более 50 элементов. Было установлено, что незаменимыми являются около 25 элементов, а это означает, что их дефицит вызывает определенные симптомы дефицита.
Важные минералы включают:
- Кальций
- фосфор
- Утюг
- Натрий
- Калий
- Хлорид-ионы
- Медь
- Кобальт
- Марганец
- Цинк
- Магний
- Фтор
- Йод
Витамины — это важные органические соединения, которые человеческий организм не может синтезировать сам по себе, и поэтому они должны присутствовать в рационе.Витамины, особенно важные для обмена веществ, включают:
- Витамин А
- B2 (рибофлавин)
- Ниацин или никотиновая кислота
- Пантотеновая кислота
Изображение предоставлено: Siberian Art / Shutterstock.com
Метаболические пути
Химические реакции метаболизма организованы в метаболические пути. Они позволяют преобразовать основные химические вещества из пищи с помощью последовательности ферментов через ряд этапов в другое химическое вещество.
Ферменты имеют решающее значение для метаболизма, потому что они позволяют организмам проводить желательные реакции, требующие энергии. Эти реакции также связаны с реакциями, высвобождающими энергию. Поскольку ферменты действуют как катализаторы, они позволяют этим реакциям протекать быстро и эффективно. Ферменты также позволяют регулировать метаболические пути в ответ на изменения в клеточной среде или сигналы от других клеток.
Список литературы
Дополнительная литература
4.1 Энергия и метаболизм — Концепции биологии — 1-е канадское издание
Цели обучения
К концу этого раздела вы сможете:
- Объясните, что такое метаболические пути
- Изложите первый и второй законы термодинамики
- Объясните разницу между кинетической и потенциальной энергией
- Описать эндергонические и экзэргонические реакции
- Обсудить, как ферменты действуют как молекулярные катализаторы
Посмотрите видео о гетеротрофах.
Ученые используют термин биоэнергетика для описания концепции потока энергии (рис. 4.2) через живые системы, такие как клетки. Клеточные процессы , такие как построение и разрушение сложных молекул , происходят посредством ступенчатых химических реакций . Некоторые из этих химических реакций являются спонтанными и высвобождают энергию, тогда как другие требуют энергии для протекания. Точно так же, как живые существа должны постоянно потреблять пищу для пополнения своих запасов энергии, клетки должны постоянно производить больше энергии, чтобы восполнить то, что используется многими химическими реакциями, требующими энергии, которые постоянно происходят.В совокупности все химические реакции , которые происходят внутри клеток, включая те, которые потребляют или генерируют энергию, называются метаболизмом клетки .
Рис. 4.2. В конечном счете, большинство форм жизни получают энергию от солнца. Растения используют фотосинтез для захвата солнечного света, а травоядные животные поедают растения для получения энергии. Плотоядные животные едят травоядных, и возможное разложение растительного и животного материала способствует пополнению запасов питательных веществ.Рассмотрим метаболизм сахара.Это классический пример одного из многих клеточных процессов, которые используют и производят энергию. Живые существа потребляют сахар в качестве основного источника энергии, потому что молекулы сахара имеют много энергии, хранящейся в их связях. По большей части фотосинтезирующие организмы, такие как растения, производят эти сахара. Во время фотосинтеза растения используют энергию (первоначально солнечного света) для преобразования газообразного углекислого газа (CO 2 ) в молекулы сахара (например, глюкозы: C 6 H 12 O 6 ).Они потребляют углекислый газ и выделяют кислород в качестве побочного продукта. Эта реакция кратко описана следующим образом:
6CO 2 + 6H 2 O + энергия ——-> C 6 H 12 O 6 + 6O 2
Поскольку этот процесс включает синтез молекулы, запасающей энергию, для его выполнения требуется подача энергии. Во время световых реакций фотосинтеза энергия обеспечивается молекулой, называемой аденозинтрифосфатом (АТФ) , которая является основным источником энергии для всех клеток.Точно так же, как доллар используется в качестве валюты для покупки товаров, клетки используют молекулы АТФ в качестве энергетической валюты для выполнения немедленной работы. Напротив, молекулы-накопители энергии, такие как глюкоза, потребляются только для того, чтобы расщепиться для использования своей энергии. Реакцию, которая собирает энергию молекулы сахара в клетках, нуждающихся в кислороде для выживания, можно описать обратной реакцией на фотосинтез. В этой реакции расходуется кислород и выделяется углекислый газ в качестве побочного продукта. Реакция резюмируется как:
C 6 H 12 O 6 + 6O 2 ——> 6CO 2 + 6H 2 O + энергия
Обе эти реакции включают много этапов.
Процессы образования и расщепления молекул сахара иллюстрируют два примера метаболических путей. Метаболический путь — это серия химических реакций, в которых исходная молекула изменяется, шаг за шагом, через ряд промежуточных продуктов метаболизма, в конечном итоге приводя к конечному продукту. В примере метаболизма сахара первый метаболический путь синтезирует сахар из более мелких молекул, а другой путь расщепляет сахар на более мелкие молекулы. Эти два противоположных процесса — первый, требующий энергии, а второй — производящий энергию — называются анаболическими путями (строительные полимеры) и катаболическими путями (расщепление полимеров на их мономеры) соответственно.Следовательно, метаболизм состоит из синтеза (анаболизма) и деградации (катаболизма) (рис. 4.3).
Важно знать, что химические реакции метаболических путей не происходят сами по себе. Каждая стадия реакции ускоряется или катализируется белком, называемым ферментом. Ферменты важны для катализирования всех типов биологических реакций — как тех, которые требуют энергии, так и тех, которые выделяют энергию.
Рис. 4.3. Катаболические пути — это те пути, которые генерируют энергию за счет разрушения более крупных молекул.Анаболические пути — это те, которые требуют энергии для синтеза более крупных молекул. Оба типа путей необходимы для поддержания энергетического баланса клетки.Термодинамика относится к изучению энергии и передачи энергии с участием физической материи. Материя, относящаяся к конкретному случаю передачи энергии, называется системой, а все, что находится вне этой материи, называется окружающей средой. Например, при нагревании кастрюли с водой на плите система включает плиту, кастрюлю и воду.Энергия передается внутри системы (между плитой, кастрюлей и водой). Есть два типа систем: открытая и закрытая. В открытой системе можно обмениваться энергией с окружающей средой. Плита открыта, потому что тепло может отдаваться воздуху. Закрытая система не может обмениваться энергией с окружающей средой.
Биологические организмы — это открытые системы. Между ними и их окружением происходит обмен энергией, поскольку они используют энергию солнца для фотосинтеза или потребляют молекулы, накапливающие энергию, и выделяют энергию в окружающую среду, выполняя работу и выделяя тепло.Как и все в физическом мире, энергия подчиняется физическим законам. Законы термодинамики управляют передачей энергии внутри и между всеми системами во Вселенной.
В общем, энергия определяется как способность выполнять работу или создавать какие-либо изменения. Энергия существует в разных формах. Например, электрическая энергия, световая энергия и тепловая энергия — это разные виды энергии. Чтобы понять, как энергия поступает в биологические системы и выходит из них, важно понимать два физических закона, управляющих энергией.
Первый закон термодинамики гласит, что общее количество энергии во Вселенной постоянно и сохраняется. Другими словами, во Вселенной всегда было и будет точно такое же количество энергии. Энергия существует во многих различных формах . Согласно первому закону термодинамики, энергия может передаваться с места на место или преобразовываться в различные формы, , но не может быть создана или уничтожена . Передачи и преобразования энергии происходят вокруг нас постоянно.Лампочки преобразуют электрическую энергию в световую и тепловую. Газовые плиты преобразуют химическую энергию природного газа в тепловую. Растения совершают одно из самых биологически полезных преобразований энергии на Земле: преобразование энергии солнечного света в химическую энергию, хранящуюся в органических молекулах (рис. 4.2). Некоторые примеры преобразования энергии показаны на рисунке 4.4.
Задача всех живых организмов — получить энергию из окружающей среды в формах, которые они могут передавать или преобразовывать в полезную энергию для выполнения работы.Живые клетки эволюционировали, чтобы справиться с этой задачей. Химическая энергия, хранящаяся в органических молекулах, таких как сахара и жиры, передается и преобразуется через ряд клеточных химических реакций в энергию в молекулах АТФ. Энергия в молекулах АТФ легко доступна для работы. Примеры типов работы, которую должны выполнять клетки, включают построение сложных молекул, транспортировку материалов, обеспечение движения ресничек или жгутиков и сокращение мышечных волокон для создания движения.
Рисунок 4.4 Показаны некоторые примеры передачи и преобразования энергии из одной системы в другую и из одной формы в другую. Пища, которую мы потребляем, обеспечивает наши клетки энергией, необходимой для выполнения функций организма, точно так же, как световая энергия дает растениям средства для создания необходимой им химической энергии. (кредит «мороженое»: модификация работы Д. Шэрон Прюитт; кредит «дети»: модификация работы Макса из Провиденса; кредитный «лист»: модификация работы Кори Занкера)Основные задачи получения живой клетки, преобразование и использование энергии для работы может показаться простым.Однако второй закон термодинамики объясняет, почему эти задачи сложнее, чем кажется. Все передачи и преобразования энергии никогда не бывают полностью эффективными . При каждой передаче энергии некоторое количество энергии теряется в непригодной для использования форме. В большинстве случаев это форма тепловой энергии. Термодинамически тепловая энергия определяется как неработающая энергия, передаваемая от одной системы к другой. Например, когда включается электрическая лампочка, часть энергии, преобразуемой из электрической энергии в энергию света, теряется в виде тепловой энергии.Точно так же часть энергии теряется в виде тепловой энергии во время клеточных метаболических реакций.
Важным понятием физических систем является понятие порядка и беспорядка. Чем больше энергии теряется системой в окружающую среду, тем менее упорядоченной и случайной является система. Ученые называют меру случайности или беспорядка в системе энтропией . Высокая энтропия означает высокий беспорядок и низкую энергию. Молекулы и химические реакции также имеют разную энтропию. Например, энтропия увеличивается, когда молекулы с высокой концентрацией в одном месте диффундируют и разлетаются.Второй закон термодинамики гласит, что энергия всегда будет теряться в виде тепла при передаче или преобразовании энергии.
Живые существа очень упорядочены, и для их поддержания в состоянии низкой энтропии требуется постоянный ввод энергии.
Когда объект находится в движении, с ним связана энергия. Подумайте о шаре для разрушения. Даже медленно движущийся шар-разрушитель может нанести большой урон другим объектам. Энергия, связанная с движущимися объектами, называется кинетической энергией (Рисунок 4.5). Ускоряющаяся пуля, идущий человек и быстрое движение молекул в воздухе (выделяющих тепло) — все они обладают кинетической энергией.
А что, если тот же самый неподвижный шар для разрушения поднять краном на два этажа над землей? Если подвешенный шар для разрушения неподвижен, связана ли с ним энергия? Ответ положительный. Энергия, которая требовалась для подъема разрушающего шара, не исчезла, но теперь сохраняется в разрушающем шаре в силу его положения и силы тяжести, действующей на него.Этот вид энергии называется потенциальной энергией (рис. 4.5). Если мяч упадет, потенциальная энергия будет преобразована в кинетическую энергию до тех пор, пока вся потенциальная энергия не будет исчерпана, когда мяч упадет на землю. Шары-разрушители тоже качаются как маятник; во время качания происходит постоянное изменение потенциальной энергии (самая высокая в верхней части качания) на кинетическую энергию (самая высокая в нижней части качания). Другие примеры потенциальной энергии включают энергию воды, удерживаемой за плотиной, или человека, который собирается прыгнуть с парашютом из самолета.
Рисунок 4.5 У негазированной воды есть потенциальная энергия; движущаяся вода, например, в водопаде или быстро текущей реке, обладает кинетической энергией. (кредит «дамба»: модификация работы «Паскаля» / Flickr; кредит «водопад»: модификация работы Фрэнка Гуалтьери)Потенциальная энергия связана не только с расположением материи, но и со структурой материи. Даже пружина на земле имеет потенциальную энергию, если она сжата; то же самое делает и туго натянутая резинка. На молекулярном уровне связи, которые удерживают атомы молекул вместе, существуют в определенной структуре, обладающей потенциальной энергией.Помните, что анаболические клеточные пути требуют энергии для синтеза сложных молекул из более простых, а катаболические пути высвобождают энергию при расщеплении сложных молекул. Тот факт, что энергия может выделяться при разрыве определенных химических связей, означает, что эти связи обладают потенциальной энергией. Фактически, в связях всех пищевых молекул, которые мы едим, хранится потенциальная энергия, которая в конечном итоге используется для использования. Это потому, что эти связи могут высвобождать энергию при разрыве.Тип потенциальной энергии, которая существует в химических связях и высвобождается при разрыве этих связей, называется химической энергией. Химическая энергия отвечает за обеспечение живых клеток энергией из пищи. Высвобождение энергии происходит при разрыве молекулярных связей в молекулах пищи.
Посмотрите видео о килокалориях.
Концепция в действии
Посетите сайт и выберите «Маятник» в меню «Работа и энергия», чтобы увидеть изменение кинетической и потенциальной энергии маятника в движении.
Узнав, что химические реакции высвобождают энергию при разрыве энергонакопительных связей, следующий важный вопрос заключается в следующем: как количественно и выражается энергия, связанная с этими химическими реакциями? Как можно сравнить энергию, выделяемую в результате одной реакции, с энергией другой реакции? Измерение свободной энергии используется для количественной оценки этой передачи энергии. Напомним, что согласно второму закону термодинамики, любая передача энергии связана с потерей некоторого количества энергии в непригодной для использования форме, такой как тепло.Свободная энергия, в частности, относится к энергии, связанной с химической реакцией, которая доступна после учета потерь. Другими словами, свободная энергия — это полезная энергия или энергия, доступная для выполнения работы.
Если во время химической реакции выделяется энергия, то изменение свободной энергии, обозначенное как ∆G (дельта G), будет отрицательным числом. Отрицательное изменение свободной энергии также означает, что продукты реакции имеют меньше свободной энергии, чем реагенты, потому что они выделяют некоторую свободную энергию во время реакции.Реакции, которые имеют отрицательное изменение свободной энергии и, следовательно, высвобождают свободную энергию, называются экзергоническими реакциями. Подумайте: ex эргономичный означает, что энергия ex в системе. Эти реакции также называются спонтанными реакциями, и их продукты имеют меньше накопленной энергии, чем реагенты. Необходимо провести важное различие между термином «спонтанный» и идеей немедленного протекания химической реакции. В отличие от повседневного использования этого термина, спонтанная реакция — это не реакция, которая возникает внезапно или быстро.Ржавчина железа — это пример спонтанной реакции, которая происходит медленно, мало-помалу, с течением времени.
Если химическая реакция поглощает энергию, а не высвобождает ее в балансе, то ∆G для этой реакции будет положительным значением. В этом случае продукты имеют больше свободной энергии, чем реагенты. Таким образом, продукты этих реакций можно рассматривать как молекулы, запасающие энергию. Эти химические реакции называются эндергоническими реакциями, и они являются несамопроизвольными .Эндергоническая реакция не будет происходить сама по себе без добавления свободной энергии.
Рисунок 4.6. Показаны некоторые примеры эндергонических процессов (требующих энергии) и экзэргонических процессов (тех, которые высвобождают энергию). (кредит a: модификация работы Натали Мэйнор; кредит b: модификация работы Министерством сельского хозяйства США; кредит c: модификация работы Кори Занкера; кредит d: модификация работы Гарри Мальша)Посмотрите на каждый из представленных процессов и решите если он эндергонический или экзэргонический.
Есть еще одна важная концепция, которую необходимо учитывать в отношении эндергонических и экзэргонических реакций. Экзергонические реакции требуют небольшого количества энергии для начала, прежде чем они смогут приступить к своим этапам высвобождения энергии. Эти реакции имеют чистое высвобождение энергии, но все же требуют некоторого ввода энергии вначале. Это небольшое количество энергии, необходимое для протекания всех химических реакций, называется энергией активации.
Концепция в действии
Посмотрите анимацию перехода от свободной энергии к переходному состоянию реакции.
Вещество, которое способствует протеканию химической реакции, называется катализатором, а молекулы, катализирующие биохимические реакции, называются ферментами. Большинство ферментов являются белками и выполняют важную задачу , снижая энергии активации химических реакций внутри клетки. Большинство реакций, критических для живой клетки, протекают слишком медленно при нормальной температуре, чтобы быть полезными для клетки. Без ферментов , чтобы ускорить эти реакции , жизнь не могла бы существовать.Ферменты делают это, связываясь с молекулами реагентов и удерживая их таким образом, чтобы облегчить процессы разрыва и образования химических связей. Важно помнить, что ферменты не изменяют, является ли реакция экзергонической (спонтанной) или эндергонической. Это потому, что они не изменяют свободную энергию реагентов или продуктов. Они только уменьшают энергию активации, необходимую для продолжения реакции (рис. 4.7). Кроме того, сам фермент не изменяется в результате реакции, которую он катализирует.После того, как одна реакция катализируется, фермент может участвовать в других реакциях.
Рис. 4.7. Ферменты снижают энергию активации реакции, но не изменяют свободную энергию реакции.Химические реагенты, с которыми связывается фермент, называются субстратами фермента. В зависимости от конкретной химической реакции может быть один или несколько субстратов. В некоторых реакциях один реагент-субстрат распадается на несколько продуктов. В других случаях два субстрата могут объединиться, чтобы создать одну большую молекулу.Два реагента также могут вступить в реакцию, и оба они станут модифицированными, но выходят из реакции в виде двух продуктов. Место внутри фермента, где связывается субстрат, называется активным участком фермента . Активный сайт — это место, где происходит «действие». Поскольку ферменты являются белками, в активном центре существует уникальная комбинация боковых цепей аминокислот. Каждая боковая цепь характеризуется разными свойствами. Они могут быть большими или маленькими, слабокислотными или основными, гидрофильными или гидрофобными, положительно или отрицательно заряженными или нейтральными.Уникальная комбинация боковых цепей создает очень специфическую химическую среду в активном центре. Эта специфическая среда подходит для связывания с одним конкретным химическим субстратом (или субстратами).
Активные сайты подвержены влиянию местной среды. Повышение температуры окружающей среды обычно увеличивает скорость реакции, катализируемой ферментами или иначе. Однако температуры, выходящие за пределы оптимального диапазона, снижают скорость, с которой фермент катализирует реакцию. Высокие температуры в конечном итоге вызовут денатурирование ферментов, необратимое изменение трехмерной формы и, следовательно, функции фермента.Ферменты также подходят для наилучшего функционирования в определенном диапазоне pH и концентрации соли, и, как и в случае с температурой, экстремальные значения pH и концентрации соли могут вызывать денатурирование ферментов.
В течение многих лет ученые считали, что связывание фермента с субстратом происходит простым способом «замок и ключ». Эта модель утверждает, что фермент и субстрат идеально сочетаются друг с другом за один мгновенный шаг. Однако текущие исследования поддерживают модель, называемую индуцированной подгонкой (рис. 4.8). Модель индуцированной подгонки расширяет модель замка и ключа, описывая более динамическое связывание между ферментом и субстратом.Когда фермент и субстрат объединяются, их взаимодействие вызывает легкий сдвиг в структуре фермента, который образует идеальную структуру связывания между ферментом и субстратом.
Концепция в действии
Просмотрите анимацию индуцированной посадки.
Когда фермент связывает свой субстрат, образуется комплекс фермент-субстрат. Этот комплекс снижает энергию активации реакции и способствует ее быстрому развитию одним из множества возможных способов. На базовом уровне ферменты способствуют химическим реакциям, в которых участвует более одного субстрата, объединяя субстраты вместе в оптимальной ориентации для реакции.Другой способ, которым ферменты способствуют реакции своих субстратов, — это создание оптимальной среды в активном центре для протекания реакции. Химические свойства, проистекающие из особого расположения R-групп аминокислот в активном центре, создают идеальную среду для реакции определенных субстратов фермента.
Комплекс фермент-субстрат может также снизить энергию активации за счет нарушения структуры связи, так что ее легче разорвать. Наконец, ферменты также могут снижать энергию активации, принимая участие в самой химической реакции.В этих случаях важно помнить, что фермент всегда возвращается в исходное состояние по завершении реакции. Одним из отличительных свойств ферментов является то, что они в конечном итоге остаются неизменными в результате катализируемых ими реакций. После того, как фермент катализирует реакцию, он высвобождает свой продукт (продукты) и может катализировать новую реакцию.
Рис. 4.8. Модель индуцированной подгонки представляет собой корректировку модели «замок-и-ключ» и объясняет, как ферменты и субстраты претерпевают динамические модификации во время переходного состояния, чтобы увеличить сродство субстрата к активному сайту.Казалось бы, идеальным иметь сценарий, в котором все ферменты организма существуют в изобилии и оптимально функционируют во всех клеточных условиях, во всех клетках, во все времена. Однако различные механизмы гарантируют, что этого не произойдет. Клеточные потребности и условия постоянно меняются от клетки к клетке и со временем меняются внутри отдельных клеток. Необходимые ферменты клеток желудка отличаются от ферментов жировых клеток, клеток кожи, клеток крови и нервных клеток. Кроме того, клетка пищеварительного органа намного усерднее обрабатывает и расщепляет питательные вещества в течение времени, которое следует за едой, по сравнению со многими часами после еды.Поскольку эти клеточные потребности и условия меняются, также должны изменяться количества и функциональность различных ферментов.
Поскольку скорость биохимических реакций контролируется энергией активации, а ферменты ниже и определяют энергии активации химических реакций, относительные количества и функционирование различных ферментов в клетке в конечном итоге определяют, какие реакции будут протекать и с какой скоростью. Это определение строго контролируется в клетках. В определенных клеточных средах активность ферментов частично контролируется факторами окружающей среды, такими как pH, температура, концентрация соли и, в некоторых случаях, кофакторами или коферментами.
Ферменты также могут регулироваться способами, которые либо способствуют, либо снижают активность фермента. Есть много видов молекул, которые подавляют или стимулируют функцию ферментов, и различные механизмы, с помощью которых они это делают. В некоторых случаях ингибирования фермента молекула ингибитора достаточно похожа на субстрат, чтобы она могла связываться с активным центром и просто блокировать связывание субстрата. Когда это происходит, фермент ингибируется посредством конкурентного ингибирования , потому что молекула ингибитора конкурирует с субстратом за связывание с активным центром.
С другой стороны, при неконкурентном ингибировании молекула ингибитора связывается с ферментом в месте, отличном от активного сайта, называемом аллостерическим сайтом , но все же удается блокировать связывание субстрата с активным сайтом. Некоторые молекулы ингибитора связываются с ферментами в том месте, где их связывание вызывает конформационное изменение, которое снижает сродство фермента к его субстрату. Этот тип торможения называется аллостерическим торможением (рис. 4.9).Большинство аллостерически регулируемых ферментов состоят из более чем одного полипептида, что означает, что они имеют более одной белковой субъединицы. Когда аллостерический ингибитор связывается с областью фермента, все активные центры белковых субъединиц слегка изменяются, так что они связывают свои субстраты с меньшей эффективностью. Есть аллостерические активаторы, а также ингибиторы. Аллостерические активаторы связываются с участками фермента, удаленными от активного сайта, вызывая конформационные изменения, которые увеличивают сродство активного сайта (ов) фермента к его субстрату (ам) (рис.9).
Рис. 4.9. Аллостерическое ингибирование работает, косвенно вызывая конформационные изменения активного сайта, так что субстрат больше не подходит. Напротив, при аллостерической активации молекула активатора изменяет форму активного центра, чтобы обеспечить лучшее прилегание субстрата.Через призму коренных народов
Растения не могут убежать или спрятаться от своих хищников, и они разработали множество стратегий, чтобы отпугнуть тех, кто их съел. Подумайте о шипах, раздражителях и вторичных метаболитах: это соединения, которые напрямую не помогают растениям расти, а созданы специально для защиты от хищников.Вторичные метаболиты — наиболее распространенный способ отпугивания хищников. Некоторые примеры вторичных метаболитов — атропин, никотин, ТГК и кофеин. Люди обнаружили, что эти вторичные метаболиты являются богатым источником материалов для лекарств. Подсчитано, что 90% лекарств в современной аптеке имеют свои «корни» в этих вторичных метаболитах.
Лечение травами первых людей открыло миру эти вторичные метаболиты. Например, коренные народы издавна использовали кору ивовых кустарников и ольхи для приготовления чая, тоника или припарок, чтобы уменьшить воспаление.Вы узнаете больше о воспалительной реакции иммунной системы в главе 11.
Рис. 4.10. Кора тихоокеанской ивы содержит соединение салицин.И ива, и кора ольхи содержат соединение салицин. У большинства из нас в аптечке есть это соединение в виде салициловой кислоты или аспирина. Доказано, что аспирин уменьшает боль и воспаление, а попав в наши клетки, салицин превращается в салициловую кислоту.
Так как это работает? Салицин или аспирин действуют как ингибитор ферментов.В воспалительной реакции ключевыми в этом процессе являются два фермента, COX1 и COX2. Салицин или аспирин специфически модифицируют аминокислоту (серин) в активном центре этих двух родственных ферментов. Эта модификация активных центров не позволяет нормальному субстрату связываться и, таким образом, нарушается воспалительный процесс. Как вы читали в этой главе, это делает его конкурентным ингибитором ферментов.
Разработчик фармацевтических препаратов
Рис. 4.11 Задумывались ли вы, как создаются фармацевтические препараты? (кредит: Дебора Остин)Ферменты — ключевые компоненты метаболических путей.Понимание того, как работают ферменты и как их можно регулировать, — ключевые принципы, лежащие в основе разработки многих фармацевтических препаратов, представленных сегодня на рынке. Биологи, работающие в этой области, совместно с другими учеными разрабатывают лекарства (рис. 4.11).
Рассмотрим, к примеру, статины. Статины — это название одного класса лекарств, которые могут снижать уровень холестерина. Эти соединения являются ингибиторами фермента HMG-CoA редуктазы, который является ферментом, синтезирующим холестерин из липидов в организме.Ингибируя этот фермент, можно снизить уровень холестерина, синтезируемого в организме. Точно так же ацетаминофен, широко продаваемый под торговой маркой Tylenol, является ингибитором фермента циклооксигеназы. Хотя он используется для снятия лихорадки и воспаления (боли), его механизм действия до сих пор полностью не изучен.
Как обнаруживаются наркотики? Одна из самых больших проблем в открытии лекарств — это определение мишени для лекарства. Мишень лекарства — это молекула, которая буквально является мишенью лекарства.В случае статинов мишенью для лечения является HMG-CoA редуктаза. Цели лекарств определяются путем кропотливых лабораторных исследований. Одной идентификации цели недостаточно; ученым также необходимо знать, как мишень действует внутри клетки и какие реакции идут наперекосяк в случае болезни. Как только цель и путь определены, начинается фактический процесс разработки лекарств. На этом этапе химики и биологи работают вместе, чтобы разработать и синтезировать молекулы, которые могут блокировать или активировать определенную реакцию.Однако это только начало: если и когда прототип лекарства успешно выполняет свою функцию, он подвергается множеству тестов, от экспериментов in vitro до клинических испытаний, прежде чем он получит одобрение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США. магазин.
Многие ферменты не работают оптимально или даже не работают, если они не связаны с другими специфическими небелковыми вспомогательными молекулами. Они могут связываться либо временно посредством ионных или водородных связей, либо навсегда посредством более прочных ковалентных связей.Связывание с этими молекулами способствует оптимальной форме и функционированию соответствующих ферментов. Двумя примерами этих типов вспомогательных молекул являются кофакторы и коферменты. Кофакторы — это неорганические ионы, такие как ионы железа и магния. Коферменты — это органические вспомогательные молекулы, имеющие базовую атомную структуру, состоящую из углерода и водорода. Подобно ферментам, эти молекулы участвуют в реакциях, не меняясь сами, и в конечном итоге перерабатываются и используются повторно. Витамины являются источником коферментов.Некоторые витамины являются предшественниками коферментов, а другие действуют непосредственно как коферменты. Витамин С является прямым коферментом множества ферментов, которые участвуют в создании важной соединительной ткани — коллагена. Следовательно, функция фермента частично регулируется обилием различных кофакторов и коферментов, которые могут поступать с пищей организма или, в некоторых случаях, вырабатываться организмом.
Рис. 4.12. Витамины являются важными коферментами или предшественниками коферментов и необходимы для правильного функционирования ферментов.Мультивитаминные капсулы обычно содержат смеси всех витаминов в разном процентном соотношении.Подавление обратной связи в метаболических путях
Молекулы могут регулировать функцию ферментов разными способами. Однако остается главный вопрос: что это за молекулы и откуда они берутся? Как вы уже знаете, некоторые из них являются кофакторами и коферментами. Какие другие молекулы в клетке обеспечивают ферментативную регуляцию, такую как аллостерическая модуляция, а также конкурентное и неконкурентное ингибирование? Возможно, наиболее подходящими источниками регуляторных молекул для ферментативного клеточного метаболизма являются продукты самих клеточных метаболических реакций.Наиболее эффективным и элегантным образом клетки эволюционировали, чтобы использовать продукты собственных реакций для подавления активности ферментов с помощью обратной связи. Подавление обратной связи предполагает использование продукта реакции для регулирования его собственного дальнейшего производства (рис. 4.12). Клетка реагирует на обилие продуктов замедлением производства во время анаболических или катаболических реакций. Такие продукты реакции могут ингибировать ферменты, которые катализируют их производство с помощью механизмов, описанных выше.
Рисунок 4.13 Метаболические пути — это серия реакций, катализируемых множеством ферментов. Ингибирование обратной связи, когда конечный продукт пути ингибирует восходящий процесс, является важным регуляторным механизмом в клетках.Производство как аминокислот, так и нуклеотидов контролируется посредством ингибирования с обратной связью. Кроме того, АТФ является аллостерическим регулятором некоторых ферментов, участвующих в катаболическом распаде сахара, процессе, который создает АТФ. Таким образом, когда АТФ в избытке, клетка может предотвратить производство АТФ.С другой стороны, АДФ служит положительным аллостерическим регулятором (аллостерическим активатором) для некоторых из тех же ферментов, которые ингибируются АТФ. Таким образом, когда относительные уровни АДФ высоки по сравнению с АТФ, клетка начинает производить больше АТФ за счет катаболизма сахара.
Клетки выполняют жизненные функции посредством различных химических реакций. Метаболизм клетки — это комбинация химических реакций, которые происходят в ней. Катаболические реакции расщепляют сложные химические вещества на более простые и связаны с выделением энергии.Анаболические процессы создают сложные молекулы из более простых и требуют энергии.
При изучении энергии термин «система» относится к веществу и окружающей среде, участвующим в передаче энергии. Энтропия — это мера беспорядка системы. Физические законы, описывающие передачу энергии, являются законами термодинамики. Первый закон гласит, что общее количество энергии во Вселенной постоянно. Второй закон термодинамики гласит, что любая передача энергии включает некоторую потерю энергии в непригодной для использования форме, такой как тепловая энергия.Энергия бывает разных форм: кинетической, потенциальной и свободной. Изменение свободной энергии реакции может быть отрицательным (высвобождает энергию, экзергонический) или положительным (потребляет энергию, эндергоническим). Все реакции требуют начального ввода энергии, называемой энергией активации.
Ферменты — это химические катализаторы, которые ускоряют химические реакции за счет снижения их энергии активации. Ферменты имеют активный центр с уникальной химической средой, которая соответствует определенным химическим реагентам для этого фермента, называемым субстратами.Считается, что ферменты и субстраты связываются в соответствии с моделью индуцированной подгонки. Действие ферментов регулируется для сохранения ресурсов и оптимального реагирования на окружающую среду.
Глоссарий
энергия активации: количество начальной энергии, необходимой для протекания реакции
активный сайт: специфическая область на ферменте, где субстрат связывается
аллостерическое ингибирование: механизм ингибирования действия фермента, в котором регуляторная молекула связывается со вторым сайтом (не активным сайтом) и инициирует изменение конформации в активном сайте, предотвращая связывание с субстратом
анаболический: описывает путь, который требует ввода чистой энергии для синтеза сложных молекул из более простых
биоэнергетика: концепция потока энергии через живые системы
катаболический: описывает путь, по которому сложные молекулы распадаются на более простые, выделяя энергию в качестве дополнительного продукта реакции.
конкурентное ингибирование: общий механизм регуляции активности фермента, при котором молекула, отличная от субстрата фермента, способна связывать активный сайт и предотвращать связывание самого субстрата, тем самым подавляя общую скорость реакции фермента
endergonic: описывает химическую реакцию, в результате которой образуются продукты, которые хранят больше химической потенциальной энергии, чем реагенты.
фермент: молекула, катализирующая биохимическую реакцию
exergonic: описывает химическую реакцию, которая приводит к продуктам с меньшей химической потенциальной энергией, чем реагенты, плюс высвобождение свободной энергии
ингибирование обратной связи: механизм регулирования активности фермента, при котором продукт реакции или конечный продукт ряда последовательных реакций ингибирует фермент на более ранней стадии в серии реакций
тепловая энергия: энергия, передаваемая из одной системы в другую, которая не работает
кинетическая энергия: тип энергии, связанной с движущимися объектами
метаболизм: все химические реакции, происходящие внутри клеток, включая те, которые используют энергию, и те, которые высвобождают энергию
неконкурентное ингибирование: общий механизм регуляции активности фермента, при котором регуляторная молекула связывается с сайтом, отличным от активного сайта, и предотвращает связывание активного сайта с субстратом; таким образом, молекула ингибитора не конкурирует с субстратом за активный центр; аллостерическое торможение — это форма неконкурентного торможения
потенциальная энергия: тип энергии, который относится к потенциалу совершать работу
субстрат: молекула, на которую действует фермент
термодинамика: наука о взаимосвязи тепла, энергии и работы
Углеводы: Продукты питания содержат углеводы в трех формах: крахмал, сахар, и целлюлоза (волокно).Крахмал и сахар очень важны источники энергии для человека. Недостаток углеводов в диета, вероятно, приведет к недостаточному количеству калорий в диете. Целлюлоза обеспечивает основную часть рациона. Поскольку ткани организма постоянно нуждаются в глюкозе, диета должна содержать такие вещества, как углеводы или вещества которые будут давать глюкозу в результате пищеварения или метаболизма. Для большинство людей в мире, более половины диеты состоит из углеводов из риса, пшеницы, хлеба, картофеля, макароны. Белки: Всей жизни нужен белок, поскольку он является главным строителем тканей. и часть каждой клетки тела. Помимо других функций, белки помочь: сделать гемоглобин в крови, который переносит кислород клетки; образуют антитела, борющиеся с инфекцией; подавать азот для генетического материала ДНК и РНК; и поставлять энергию. Белки необходимы для питания, потому что они содержат аминокислоты.Среди 20 или более аминокислот человеческий организм не может синтезировать 8, поэтому эти аминокислоты называют незаменимые аминокислоты. Пища, содержащая белок, может быть плохой биологическая ценность, если он недостаточен в одном или нескольких из 8 основных аминокислоты: лизин, триптофан, метионин, лейцин, изолейцин, фенилаланин, валин и треонин. Белки животного происхождения имеют наивысшую биологическую ценность, поскольку содержат больше количество незаменимых аминокислот.Еда лучшего качества белки перечислены в порядке убывания качества: цельные яйца, молоко, соевые бобы, мясо, овощи и зерновые. Жиры и липиды: Жиры являются концентрированными источниками энергии, потому что они дают вдвое больше энергии, чем углеводы или белки на весовая основа. Функции жиров: входить в состав структура ячеек, образующих защитную подушку и теплоизоляцию вокруг жизненно важных органов, переносят жирорастворимые витамины и обеспечивают резервный накопитель энергии. Три незаменимых ненасыщенных жирных кислоты включают:
линолевая, линолиновая и арахидоновая и имеют 2, 3 и 4 двойных
облигации соответственно. Насыщенные жиры, наряду с холестерином, имеют
были замешаны в артериосклерозе, «затвердевании артерий».
По этой причине в рационе следует сократить насыщенные жиры.
(животные) и с повышенным содержанием ненасыщенных жиров (растительные). б) ADP + P + энергия —> ATP + H 2 O |
Обзор Метаболизм
Введение:
Углеводный обмен начинается с переваривания в малых кишечник, где моносахариды всасываются в кровоток.Концентрация сахара в крови контролируется тремя гормонами: инсулин, глюкагон и адреналин. Если концентрация глюкозы в крови слишком много, инсулин секретируется поджелудочной железой. Инсулин стимулирует перенос глюкозы в клетки, особенно в печени и мышцах, хотя другие органы также могут метаболизировать глюкозу.
В печени и мышцах большая часть глюкозы превращается в гликоген в процессе гликогенеза (анаболизм).Гликоген хранится в печени и мышцах, пока не понадобится позже время, когда уровень глюкозы низкий. Если уровень глюкозы в крови низкий, то гормоны экинефрина и глюкогона секретируются для стимуляции превращение гликогена в глюкозу. Этот процесс называется гликогенолиз (катаболизм).
Если глюкоза необходима сразу после попадания в клетки поставляя энергию, он начинает метаболический процесс, называемый гликоизом (катаболизм).Конечными продуктами гликолиза являются пировиноградная кислота. и ATP .
Поскольку гликолиз высвобождает относительно мало АТФ, дальнейшие реакции продолжить преобразование пировиноградной кислоты в ацетил-КоА, а затем в лимонную кислота в цикле лимонной кислоты. Большая часть АТФ производится от окислений в цикле лимонной кислоты в связи с электронная транспортная цепь.
При напряженной мышечной деятельности пировиноградная кислота преобразуется в молочную кислоту, а не в ацетил-КоА.Во время отдыха период, молочная кислота превращается обратно в пировиноградную кислоту. В пировиноградная кислота, в свою очередь, превращается обратно в глюкозу в процессе называется глюконеогенез (анаболизм). Если глюкоза в этот момент он не нужен, он превращается в гликоген в результате гликогенеза. Вы можете вспомнить эти термины, если подумаете о «генезисе». как начало формирования.
Эти процессы кратко изложены в сводке Metaboism в рисунок слева.Каждый из этих процессов будет развиваться более подробно различные страницы этого модуля.
Метаболизм: мифы и факты
Метаболизм относится к биохимическим процессам, которые происходят в любом живом организме, включая человека, для поддержания жизни.
Эти биохимические процессы позволяют людям расти, воспроизводить, восстанавливать повреждения и реагировать на окружающую среду.
Принято считать, что у худых людей метаболизм выше, а у людей с избыточным весом — медленнее.На самом деле это случается очень редко.
В этой статье Центра знаний MNT будут обсуждаться факты, лежащие в основе метаболизма, что это такое, что он делает и как на него влияет.
Краткие сведения о метаболизме:
- Когда люди используют слово «метаболизм», они часто имеют в виду катаболизм и анаболизм.
- Катаболизм — это расщепление соединений с высвобождением энергии.
- Анаболизм — это построение соединений с использованием энергии.
- Вес тела человека является результатом катаболизма минус анаболизм.
Несмотря на то, что говорят сторонники определенных марок «здоровой» пищи, люди мало что могут сделать, чтобы существенно изменить уровень метаболизма в состоянии покоя.
Долгосрочные стратегии, такие как увеличение мышечной массы, в конечном итоге могут дать эффект.
Однако определение энергетических потребностей организма и соответствующая адаптация образа жизни быстрее повлияет на изменение массы тела.
Большинство людей неправильно используют термин «метаболизм» для анаболизма или катаболизма:
Анаболизм — это построение вещей — последовательность химических реакций, в результате которых молекулы образуются из более мелких компонентов; анаболические процессы обычно требуют энергии.
Катаболизм — это распад вещей — серия химических реакций, которые расщепляют сложные молекулы на более мелкие единицы; катаболические процессы обычно высвобождают энергию.
Анаболизм
Анаболизм позволяет организму выращивать новые клетки и поддерживать все ткани. В анаболических реакциях в организме используются простые химические вещества и молекулы для производства многих готовых продуктов. Примеры включают рост и минерализацию костей и увеличение мышечной массы.
Классические анаболические гормоны включают:
- Гормон роста — гормон, вырабатываемый гипофизом и стимулирующий рост.
- Инсулин — гормон, вырабатываемый поджелудочной железой. Он регулирует уровень сахара в крови. Клетки не могут использовать глюкозу без инсулина.
- Тестостерон — вызывает развитие мужских половых признаков, таких как более глубокий голос и растительность на лице. Он также укрепляет мышцы и кости.
- Эстроген — участвует в укреплении костной массы, а также в развитии женских качеств, таких как грудь.
Катаболизм
Катаболизм разрушает вещи и высвобождает энергию; он использует более крупные соединения для создания более мелких соединений, высвобождая при этом энергию.Катаболизм обеспечивает организм энергией, необходимой для физической активности, от клеточных процессов до движений тела.
Катаболические реакции в клетках расщепляют полимеры (длинные цепочки молекул) на их мономеры (отдельные звенья). Например:
- Полисахариды расщепляются на моносахариды — например, крахмал расщепляется на глюкозу.
- Нуклеиновые кислоты расщепляются на нуклеотиды — нуклеиновые кислоты, такие как те, что составляют ДНК, расщепляются на пурины, пиримидины и пентозные сахара.Они участвуют в снабжении организма энергией.
- Белки расщепляются на аминокислоты — в некоторых случаях белок расщепляется на аминокислоты с образованием глюкозы.
Когда мы едим, наш организм расщепляет питательные вещества — это высвобождает энергию, которая хранится в молекулах аденозинтрифосфата (АТФ) в организме. АТФ считается «энергетической валютой жизни».
Энергия, запасенная в АТФ, является топливом для анаболических реакций. Катаболизм создает энергию, которую анаболизм потребляет для синтеза гормонов, ферментов, сахаров и других веществ, необходимых для роста, размножения и восстановления клеток.
Масса тела — это результат катаболизма минус анаболизм — количество энергии, которое мы выделяем в наши тела (катаболизм), минус количество энергии, потребляемой нашим телом (анаболизм).
Избыточная энергия сохраняется в мышцах и печени в виде жира или гликогена. Гликоген — это основная форма хранения глюкозы в организме.
Один грамм жира дает 9 калорий по сравнению с 4 калориями из грамма белка или углеводов.
Хотя избыточный вес является результатом накопления организмом избыточной энергии в виде жира, иногда гормональные проблемы или основное заболевание могут влиять на обмен веществ.
Если кто-то страдает избыточным весом или ожирением, рекомендуется пройти медицинское обследование, чтобы определить, влияет ли заболевание на массу тела.
Как рассчитать массу тела с использованием ИМТ (индекса массы тела)
ИМТ — это основанный на фактах способ расчета идеальных диапазонов массы тела для возраста и роста. Для расчета ИМТ CDC предоставляет Калькулятор ИМТ для взрослых.
Существует множество способов определения индивидуальных потребностей в калориях, в том числе следующие:
Размер и состав тела
Для увеличения массы тела требуется больше калорий.Людям с большей мышечной массой по сравнению с жиром потребуется больше калорий, чем людям, которые весят столько же, но имеют меньше мышц по сравнению с жиром.
Следовательно, люди с более высоким соотношением мышечного жира имеют более высокий базальный уровень метаболизма, чем люди с более низким соотношением мышечного жира, если их вес такой же.
Возраст
По мере того, как люди стареют, появляется несколько факторов, которые приводят к снижению потребности в калориях. Мышечная масса падает, что приводит к увеличению соотношения жиров и мышц. Кроме того, следующие возрастные факторы снижают потребность человека в калориях:
- Гормоны — мужчины вырабатывают меньше тестостерона, а женщины вырабатывают меньше эстрогена с возрастом — оба гормона участвуют в анаболических процессах, которые потребляют энергию.
- Менопауза — по мере приближения женщины к менопаузе наблюдается снижение уровня гормонов, которые обычно способствуют использованию энергии. Многим женщинам в это время труднее похудеть.
- Физическая активность — пожилые люди обычно менее физически активны, чем в молодости.
- Пол — у мужчин более высокий уровень метаболизма, чем у женщин, потому что у них выше соотношение мышечной массы и жира. Это означает, что средний мужчина будет сжигать больше калорий, чем среднестатистическая женщина того же возраста и веса.
После определения потребности в калориях и подтверждения отсутствия основного состояния, способствующего увеличению веса, лучшим подходом будет сосредоточение внимания на трех важнейших факторах; это:
Высыпание
Недостаток сна может способствовать нарушению нейроэндокринного контроля аппетита. Это может привести к перееданию, изменению инсулинорезистентности и повышенному риску развития диабета 2 типа — все это может привести к увеличению веса.
Несколько исследований показали, что лишение сна нарушает способность организма регулировать прием пищи за счет снижения уровня лептина, гормона, который сообщает организму, когда он сыт.
Получение достаточного количества физических упражнений
В ходе 6-месячного исследования, проведенного исследователями из Медицинского центра Университета Дьюка, изучалось влияние физических упражнений на 53 участника, ведущих малоподвижный образ жизни.
В ходе испытания измерялось влияние четырех уровней физической активности: эквивалент 12 миль ходьбы в неделю, 12 миль бега в неделю, 20 миль бега в неделю и бездействия.
Значительные улучшения были отмечены в группах упражнений. Важно отметить, что для достижения положительных результатов требовалось лишь умеренное количество упражнений.
Улучшение диеты и питания
Лучший способ улучшить диету и питание — это есть много фруктов и овощей. Управление количеством калорий, потребляемых каждый день, является важным фактором контроля веса, особенно при попытке похудеть.
Однако было доказано, что строгое ограничение калорий неэффективно для долгосрочного успеха. Резкое снижение калорийности может вызвать изменение метаболизма в организме, в результате чего будет сжигаться гораздо меньше энергии, и в то же время накапливаться любая энергия, которую он может найти.Очень низкокалорийные диеты обычно подрывают мотивацию, что приводит к перееданию при отказе от диеты.
Если только очень низкокалорийная диета не контролируется высококвалифицированным диетологом, диетологом или врачом, существует значительный риск недоедания, которое не только вредно для здоровья, но также может повлиять на метаболизм таким образом, чтобы добиться похудения труднее.
Метаболизм — канал улучшения здоровья
Метаболизм — это все химические процессы, постоянно происходящие внутри вашего тела, которые обеспечивают жизнь и нормальное функционирование (поддержание нормального функционирования в организме называется гомеостазом).Эти процессы включают те, которые расщепляют питательные вещества из нашей пищи, и те, которые строят и восстанавливают наше тело.
Для построения и восстановления тела требуется энергия, которая в конечном итоге поступает из пищи.
Количество энергии, измеряемое в килоджоулях (кДж), сжигаемое вашим телом в любой момент времени, зависит от вашего метаболизма.
Достижение или поддержание здорового веса — это баланс. Если мы регулярно едим и выпиваем больше килоджоулей, чем необходимо для нашего метаболизма, мы сохраняем его в основном в виде жира.
Большая часть энергии, которую мы используем каждый день, используется для того, чтобы все системы нашего тела функционировали должным образом. Это вне нашего контроля. Однако, когда мы тренируемся, мы можем заставить метаболизм работать на нас. Когда вы активны, тело сжигает больше энергии (килоджоулей).
Наш метаболизм сложен — попросту говоря, он состоит из двух частей, которые тщательно регулируются организмом, чтобы обеспечить их баланс. Это:
- Катаболизм — расщепление пищевых компонентов (таких как углеводы, белки и пищевые жиры) на их более простые формы, которые затем можно использовать для получения энергии и основных строительных блоков, необходимых для роста и восстановления.
- Анаболизм — часть метаболизма, в которой наш организм строится или восстанавливается. Анаболизм требует энергии, которая в конечном итоге поступает из нашей пищи. Когда мы едим больше, чем нам необходимо для ежедневного анаболизма, избыток питательных веществ обычно откладывается в нашем теле в виде жира.
Скорость метаболизма (или общий расход энергии) вашего тела можно разделить на три компонента:
- Базальная скорость метаболизма (BMR) — даже в состоянии покоя организму требуется энергия (килоджоули) для поддержания функционирования всех его систем. правильно (например, дыхание, поддержание сердцебиения для циркуляции крови, рост и восстановление клеток и регулировка уровня гормонов).BMR тела составляет наибольшее количество энергии, расходуемой ежедневно (50–80 процентов от вашего ежедневного потребления энергии).
- Термический эффект пищи (также известный как термогенез) — ваше тело использует энергию для переваривания потребляемых вами продуктов и напитков, а также поглощает, транспортирует и сохраняет их питательные вещества. На термогенез приходится около 5–10 процентов потребляемой вами энергии.
- Энергия, используемая во время физической активности — это энергия, используемая при физическом движении, и она наиболее сильно зависит от того, сколько энергии вы потребляете каждый день.Физическая активность включает запланированные упражнения (например, пробежку или занятия спортом), но также включает в себя все побочные действия (например, развешивание белья, игры с собакой или даже ерзание!).
В расчете на умеренно активного человека (30–45 минут физической активности умеренной интенсивности в день), этот компонент составляет 20 процентов нашего ежедневного потребления энергии.
Основная скорость метаболизма (BMR)
BMR означает количество энергии, необходимое вашему организму для поддержания гомеостаза.
Ваш BMR в значительной степени определяется вашей общей мышечной массой, особенно мышечной массой, потому что для поддержания мышечной массы требуется много энергии. Все, что снижает мышечную массу, снижает ваш BMR.
Поскольку на ваш BMR приходится значительная часть вашего общего потребления энергии, важно сохранить или даже увеличить мышечную массу с помощью упражнений при попытке похудеть.
Это означает сочетание упражнений (особенно упражнений с отягощением и отягощениями для увеличения мышечной массы) с изменениями в сторону более здорового режима питания, а не только с изменениями питания, поскольку употребление слишком малого количества килоджоулей стимулирует организм замедлять метаболизм для сохранения энергии.
Поддержание сухой мышечной массы также помогает снизить вероятность травм во время тренировок, а упражнения увеличивают ежедневные затраты энергии.У среднего мужчины BMR составляет около 7 100 кДж в день, в то время как у средней женщины BMR составляет около 5 900 кДж в день. Расход энергии постоянный, но скорость меняется в течение дня. Уровень расхода энергии обычно самый низкий ранним утром.
Факторы, влияющие на наш BMR
На ваш BMR влияют несколько факторов, работающих в сочетании, в том числе:
- Размер тела — более крупные взрослые тела имеют больше метаболизирующих тканей и больший BMR.
- Количество безжировой мышечной ткани — мышцы быстро сжигают килоджоули.
- Количество жира в организме — жировые клетки «вялые» и сжигают гораздо меньше килоджоулей, чем большинство других тканей и органов тела.
- Экстренная диета, голодание или голодание — потребление слишком небольшого количества килоджоулей стимулирует организм замедлять метаболизм для сохранения энергии. BMR может снизиться до 15 процентов, и если также будет потеряна мышечная ткань, это еще больше снизит BMR.
- Возраст — метаболизм замедляется с возрастом из-за потери мышечной ткани, а также из-за гормональных и неврологических изменений.
- Рост — младенцы и дети имеют более высокие энергетические потребности на единицу массы тела из-за энергетических потребностей роста и дополнительной энергии, необходимой для поддержания температуры тела.
- Пол — как правило, у мужчин более быстрый метаболизм, потому что они, как правило, крупнее.
- Генетическая предрасположенность — ваш метаболизм может частично определяться вашими генами.
- Гормональный и нервный контроль — BMR контролируется нервной и гормональной системами. Гормональный дисбаланс может влиять на то, как быстро или медленно организм сжигает килоджоули.
- Температура окружающей среды — если температура очень низкая или очень высокая, организму приходится усерднее работать, чтобы поддерживать нормальную температуру тела, что увеличивает BMR.
- Инфекция или болезнь — BMR увеличивается, потому что организму приходится усерднее работать, чтобы построить новые ткани и создать иммунный ответ.
- Объем физической активности — трудолюбивым мышцам нужно много энергии для сжигания. Регулярные упражнения увеличивают мышечную массу и учит тело сжигать килоджоули быстрее, даже в состоянии покоя.
- Наркотики, такие как кофеин или никотин, могут увеличивать BMR.
- Недостаточное питание — например, диета с низким содержанием йода снижает функцию щитовидной железы и замедляет обмен веществ.
Термический эффект пищи
Ваш BMR повышается после еды, потому что вы используете энергию для еды, переваривания и метаболизма только что съеденной пищи. Повышение происходит вскоре после того, как вы начинаете есть, и достигает пика через два-три часа.
Это повышение BMR может составлять от 2 до 30 процентов, в зависимости от размера еды и типов съеденных продуктов.
Различные продукты повышают BMR на разную величину. Например:
- Жиры повышают BMR на 0–5 процентов.
- Углеводы повышают BMR на 5–10 процентов.
- Белки повышают BMR на 20–30%.
- Горячие острые продукты (например, продукты, содержащие перец чили, хрен и горчицу) могут иметь значительный термический эффект.
Энергия, используемая во время физической активности
Во время напряженной или энергичной физической активности наши мышцы могут сжигать до 3000 кДж в час.Энергетический расход мышц составляет только 20 процентов от общего расхода энергии в состоянии покоя, но во время напряженных упражнений он может увеличиваться в 50 или более раз.Энергия, используемая во время упражнений, — это единственная форма расхода энергии, которую мы можем контролировать.
Однако оценить энергию, потраченную во время упражнений, сложно, поскольку истинное значение для каждого человека будет варьироваться в зависимости от таких факторов, как их вес, возраст, состояние здоровья и интенсивность, с которой выполняется каждое действие.
Австралия имеет руководящие принципы физической активности, которые рекомендуют количество и интенсивность активности в зависимости от возраста и стадии жизни. Для нашего общего здоровья важно ограничивать время, в течение которого мы ведем малоподвижный образ жизни (сидеть или бездельничать), и обеспечивать как минимум 30 минут физической активности умеренной интенсивности каждый день.
В качестве приблизительного ориентира:
- Умеренная физическая нагрузка означает, что вы можете говорить во время тренировки, но не можете петь.
- Энергичные упражнения означают, что вы не можете говорить и заниматься одновременно.
Мышечная ткань имеет большой аппетит к килоджоулей. Чем больше у вас мышечной массы, тем больше килоджоулей вы сожжете.
Люди склонны полнеть с возрастом, отчасти потому, что тело медленно теряет мышцы. Неясно, является ли потеря мышечной массы результатом процесса старения или потому, что многие люди с возрастом становятся менее активными. Однако, вероятно, это больше связано с уменьшением активности. Исследования показали, что силовые тренировки и тренировки с отягощениями могут уменьшить или предотвратить потерю мышечной массы.
Если вам больше 40 лет, у вас уже есть какое-либо заболевание или вы какое-то время не тренировались, обратитесь к врачу перед началом новой фитнес-программы.
Гормоны помогают регулировать метаболизм. Некоторые из наиболее распространенных гормональных нарушений влияют на щитовидную железу. Эта железа выделяет гормоны, регулирующие многие метаболические процессы, включая расход энергии (скорость, с которой сжигаются килоджоули).
Заболевания щитовидной железы включают:
- Гипотиреоз (недостаточная активность щитовидной железы) — метаболизм замедляется из-за того, что щитовидная железа не вырабатывает достаточное количество гормонов.Частая причина — аутоиммунное заболевание Хашимото. Некоторые из симптомов гипотиреоза включают необычную прибавку в весе, вялость, депрессию и запор.
- Гипертиреоз (сверхактивная щитовидная железа) — железа выделяет большее количество гормонов, чем необходимо, и ускоряет обмен веществ. Наиболее частой причиной этого состояния является болезнь Грейвса. Некоторые из симптомов гипертиреоза включают повышенный аппетит, потерю веса, нервозность и диарею.
Наши гены — это схемы белков в нашем организме, а наши белки отвечают за пищеварение и метаболизм нашей пищи.
Иногда дефектный ген означает, что мы производим белок, который неэффективен для обработки нашей пищи, что приводит к нарушению обмена веществ. В большинстве случаев генетические нарушения обмена веществ можно лечить под наблюдением врача, уделяя особое внимание диете.
Симптомы генетических нарушений обмена веществ могут быть очень похожи на симптомы других нарушений и заболеваний, что затрудняет установление точной причины. Обратитесь к врачу, если подозреваете, что у вас нарушение обмена веществ.
Некоторые генетические нарушения обмена веществ включают:
- Непереносимость фруктозы — неспособность расщеплять фруктозу, тип сахара, который содержится во фруктах, фруктовых соках, сахаре (например, тростниковом сахаре), меде и некоторых овощах. .
- Галактоземия — неспособность превратить углеводную галактозу в глюкозу. Сама по себе галактоза в природе не встречается. Он вырабатывается, когда пищеварительная система расщепляет лактозу на глюкозу и галактозу. Источники лактозы включают молоко и молочные продукты, такие как йогурт и сыр.
- Фенилкетонурия (PKU) — неспособность превращать аминокислоту фенилаланин в тирозин. Высокий уровень фенилаланина в крови может вызвать повреждение головного мозга.Следует избегать продуктов с высоким содержанием белка и тех, которые содержат искусственный подсластитель аспартам.
Куда обратиться за помощью
Фармакологический метаболизм — обзор
5.33.6.2 Программы прогнозирования метаболитов
Метаболизм, по сути, представляет собой серию химических реакций, каждая из которых связана с субстратом и продуктами. Компьютерная система, способная распознавать химические структуры и отображать продукты метаболизма, является идеальным инструментом для поддержки исследований и разработок лекарственных средств.Требования к такой системе можно определить следующим образом:
- •
способность вводить новые химические структуры;
- •
содержит доступные сведения обо всех возможных метаболических реакциях, подтвержденные примерами;
- •
содержит правила или вспомогательную информацию, которая позволяет различать вероятные, возможные и маловероятные метаболиты;
- •
способен предупреждать о реакциях, в которых могут образовываться реактивные промежуточные продукты, обладающие потенциалом токсичности; и
- •
предупреждают о возможных межвидовых различиях в возможных реакциях или видоспецифических реакциях.
Были разработаны и предоставлены различные программы, но все они все еще находятся на относительно низком уровне сложности. К ним относятся METEOR, 42 MetabolExpert, 43 META, 44 и недавно представленный MetaDrug 45 (таблица 3). Все они номинально действуют одинаково механически, хотя существуют различия в знаниях и правилах, используемых для получения прогноза.
Таблица 3. Доступные в настоящее время программы прогнозирования метаболитов
| Программное обеспечение | Производитель и веб-сайт | |
|---|---|---|
| META | MultiCASE Inc. | |
| http://www.multicase.com | ||
| MetabolExpert | CompuDrug Inc. | |
| http://www.compudrug.com | ||
| METEOR 03663 | http://www.lhasalimited.org | |
| MetaSite | Molecular Discovery Ltd | |
| http://www.moldiscovery.com | ||
| MetaDrug | GeneCo Inc. | |
| http://www.geneco.com |
METEOR — это программа, разработанная для прогнозирования структур вероятных метаболитов на основе оценки встроенных правил взаимоотношений структура – метаболизм. 46 В ходе его разработки было признано, что необходимо иметь некоторую основу для предсказания наиболее вероятных метаболитов, а не всех теоретически возможных. Это было достигнуто с помощью интегрированного механизма рассуждений, основанного на системе нечисловой аргументации. 47 В соответствии с заранее заданными уровнями абсолютной и относительной категоризации вероятности реакций и ссылкой на расчет log P , метаболиты могут быть предсказаны для пяти различных уровней, а именно «вероятный», «правдоподобный», «сомнительный». сомневаюсь »и« невероятно », которые можно выбрать заранее. Кроме того, можно выбрать количество последовательных стадий реакции фазы I, что снижает комбинаторный взрыв метаболитов, который может возникнуть при наличии множества различных потенциальных участков метаболизма.Составные части запроса могут быть построены с использованием связанной программы для рисования структур или импортированного molfile. Можно просмотреть результаты, которые показывают структуру метаболита с выделением места реакции. Когда происходит расщепление молекулы, показаны оба продукта. Недавняя оценка его эффективности была опубликована для 10 субстратов, основные метаболиты которых были известны. 48 Для этих субстратов 130 метаболитов первого поколения были предсказаны и / или идентифицированы экспериментально. Из них 30% были верными прогнозами, 62% — явно ложноположительными и 8% — ложноотрицательными.Следовательно, 70% можно было бы считать неправильными, включая 20% ложноположительных результатов из-за неучтенных молекулярных ограничений, 3% ложноотрицательных результатов из-за отсутствия реакций в базе данных, а остальное — из-за сложности биологических факторов. Использование этого типа оценки может помочь улучшить систему.
MetabolExpert использует базу знаний, которая для каждого преобразования содержит подструктуру, структуру продукта, список подструктур, которые должны присутствовать, чтобы реакция произошла, и список подструктур, присутствие которых предотвращает преобразование.Количество уровней превращений фазы I может быть выбрано, и когда образуется метаболит фазы II, дальнейшие преобразования не выполняются. Он работает двумя способами, а именно составляет метаболическое дерево путем сопоставления известных биотрансформаций для соответствующих субструктур и функциональных групп в молекуле или путем проведения аналогии с информацией в базе данных о структурно подобных соединениях. Перечисляются аналоги, доступные для сравнения, и можно выбрать тот, который использовался. Этот способ работы очень похож на использование одной из баз данных знаний, хотя они неизбежно будут содержать более обширные данные.Базовая база данных биотрансформации версии 10.0 содержит 179 преобразований. Существует также версия под названием RetroMex, которая направлена на прогнозирование субстратов, которые будут генерировать определенное соединение в результате метаболизма.
META, как сообщается, была собрана, начав с компиляции основных ферментов, участвующих в метаболизме, и оценки структурных сайтов и их активности для каждого из них. Правила, определяющие их применение к конкретным структурам, хранятся в серии логически связанных словарей.Программа работает на основе распознавания целей и последующих преобразований из входной структуры, которая может быть кодом SMILES или, что более вероятно, molfile. Каждая цель / преобразование получает значение приоритета. Включен модуль стабильности, который проверяет, является ли первичный молекулярный объект стабильным или он самопроизвольно разлагается до стабильного конечного продукта. Программа может использоваться для перехода к последовательным уровням метаболизма. Сообщается, что словарь реакций содержит более 1000 преобразований, охватывающих активность 30 различных ферментных систем, и более 300 преобразований в модуле стабильности.
MetaDrug сочетает в себе предсказание метаболитов на основе правил, количественные модели структуры и метаболизма для основных ферментов, метаболизирующих лекарства, и инструменты генной сети. Учитывая его новизну, необходимы независимые проверки, прежде чем можно будет оценить его потенциал.
Трудно судить о достоинствах этих существующих систем, равно как и сравнивать их производительность в этой главе. Неуместно сравнивать количество превращений, которые каждая содержит, поскольку субструктура / функциональные группы, относящиеся к реакции, могут быть определены очень конкретно или более широко.Справедливая оценка их относительной эффективности была бы тщательным упражнением, сравнивая предсказания с экспериментальными данными для широкого диапазона соединений. Нет сомнений в том, что было бы относительно легко показать, что каждый из них показал хорошие результаты для одного соединения и одинаково плохо для другого. Но ни одну систему нельзя осуждать на основании одного неверного прогноза. Общая производительность зависит от качества и глубины знаний, которые каждый содержит, что может быть оценено только путем обширной оценки.Возникает вопрос, как количественно оценить эффективность системы прогнозирования метаболитов. Цель состоит в том, чтобы предсказать только те метаболиты, которые образуются. Предложить структуры 20 метаболитов, чтобы предсказать четыре, которые действительно производятся, в большинстве случаев бесполезно, и, наоборот, предложить четыре метаболита и предсказать только один из четырех, которые производятся, также не является высоким показателем успеха. Таким образом, необходимо рассмотреть два критерия и возможные определения:
коэффициент предсказания = C / A
индекс эффективности = C / B
, где A — общее количество экспериментально образованных метаболитов, B — это общее количество предсказанных метаболитов, а C — это общее количество правильно предсказанных метаболитов.Целевой показатель для обоих этих параметров равен единице.
Можно утверждать, что коэффициент предсказания является наиболее важным критерием. А именно, что ложные срабатывания менее важны, чем пропуск истинных срабатываний. Ясно, что мы не можем ожидать этого на данном этапе, но любую программу можно постоянно улучшать, если будут включены современные знания и разработаны новые правила.